تکنیک واکنش زنجیره ای پلیمراز (PCR)
✍PCR چیست و چه کاربردهایی دارد؟
PCR، روشی غیر از کلون سازی است که مقادیر نامحدودی از توالی موردنظر را تولید می کند
این تکنیک برای بررسی حضور یا عدم حضور یک ژن خاص در مخلوطی از DNA ها، تشخیص های قبل از تولد (تعیین جنسیت، بیماری ها) و… استفاده می شود. تکنیک PCR همان همانندسازی در شرایط in vitro است در واقع یعنی تکثیر آنزیمی یک قطعه از DNA که بین دو الیگونوکلئوتید (پرایمرها) قرار گرفته بنابراین باید با به کارگیری علم بیوانفورماتیک توالی اطراف قطعه مورد نظرمان را پیدا کنیم و با طراحی پرایمر برای آنها و اعمال سیکل های مکرر حرارتی قطعه را تکثیر کنیم.
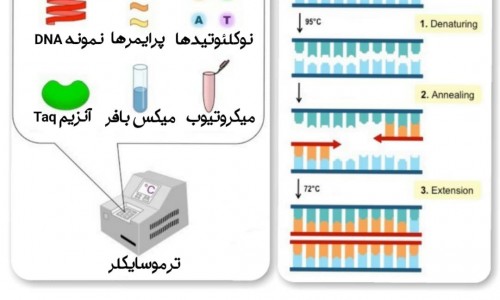
بعد از استخراج DNA که در مطالب قبل گفته شد، یک سری مواد و وسایل برای PCR لازم داریم مثل: بافر، آنزیم ،MgCl2 ،dNTP، پرایمر،آنزیم DNA پلیمراز Taq یا Pfu مقاوم به حرارت و .. و DNA الگو که همه ی این مواد و در تیوب مخصوص ریخته و در دستگاه ترکوسایکلر که سیکل های مکرر حرارتی اعمال می کند قرار می دهیم.
مراحل یک سیکل PCR:
به هر سیکل از PCR یک Stage گفته می شود که هر Stage شامل چندین Step می باشد.
مرحله واسرشت (Denaturation Step): مرحله باز شدن دو رشته DNA ، که در این مرحله دمای دستگاه را معمولا تا دمای ۹۴ تا ۹۸ درجه سانتیگراد بالا برده که این دما باعث گسستن پیوند های هیدروژنی دو رشته DNA و نهایتا دناتوره شدن مولکول می شود. حرارت در این مرحله به میزان نوکلئوتیدها در DNA بستگی دارد.
مرحله اتصال (Annealing Step): در این مرحله حرارت تا دمای ۵۵-۶۵ درجه سانتیگراد پایین می آید ، در این مرحله پرایمرهای موجود در مخلوط واکنش در محل های ویژه ای از مولکول DNA اتصال پیدا می کنند. البته در این دما امکان دو رشته ای شدن مجدد DNA وجود دارد ولی عمدتا این اتفاق رخ نمی دهد.
مرحله پليمريزاسيون یا طویل شدن (Extension/Elongation Step): در مرحله سوم دوباره دمای دستگاه تا ۷۲ درجه سانتیگراد افزایش پیدا می کند که این دما مناسب ترین حرارت برای عملکرد صحیح آنزیم DNA پلیمراز Taq موجود در مخلوط واکنش است. در اینجا وظیفه آنزیم پلیمراز این است که به هر پرایمر بچسبد و از DNA الگو رشته جدیدی بسازد.
مراحل بعد در واکنش زنجیره ای پلیمراز در واقع تکرار تمام این مراحل از ابتدا تا انتها است به طوری که با تکرار به میزان ۲۵ تا ۴۰ چرخه، میزان DNA کپی شده به بیش از ۱۳۰ میلیون مولکول DNA دو رشته ایی می رسد.
مرحله طویل شدن نهایی (Final Elongation): این مرحله، پس از آخرین سیکل PCR در دمای ۷۲ درجه انجام می شود، تا اطمینان حاصل شود که همه تک رشته های DNA همانند سازی شده اند.
نگهداری نهایی (Final hold): در این مرحله، محلول نهایی به مدت کوتاهی در دمای ۴ الی ۱۵ درجه قابل نگهداری است.
در نهایت می توانیم صحت انجام PCR را از طریق الکتروفورز در ژل آگارز یا پلی اکریل امید بررسی کنیم.
نوشته شده توسط داروینو در تاریخ ۰۰/۰۴/۲۱ ساعت ۱۵:۲۷ | تعداد دیدگاهها: ۰ دیدگاه | دستهبندی: بلاگ | برچسبها: آنزیم_DNA_پلیمراز_Taq, تکنیک_PCR, تکنیک_واکنش_زنجیره_ای_پلیمراز, تکنیک_واکنش_زنجیره_ای_پلیمراز_PCR, دوره_آموزشی_ژنتیک_مولکولی, دوره_کارآموزی_مولکولار_ژنتیک, راهنمی_آموزشی_تکنیک_واکنش_زنجیره_ای_پلیمرازPCR_, رفع_اشکالات_PCR, رفع_اشکالات_تکنیک_واکنش_زنجیره_ای_پلیمراز, شرایط_in_vitro, مبانی_و_مفاهیم_تکنیک_واکنش_زنجیره_ای_پلیمرازPCR_, ژل_آگارز, ژل_پلی_اکریل_امید, کارگاه_آموزشی__آنالیز_داده_ها_در_آزمایشگاه_ژنتیک