SDS-PAGE چیست؟
تکنیک SDS-PAGE روشی است با هزینه کم، سریع و تکرار پذیر برای مطالعه پروتئین ها. تکنیک SDS-PAGE در واقع یک روش الکتروفورز ژل است که برای جداسازی پروتئین معمولاً در بیوشیمی، ژنتیک، پزشکی قانونی و زیست شناسی مولکولی استفاده می شود. رایجترین فناوری مورد استفاده جهت تحلیل و بررسی مراحل خالص سازی و همچنین تعیین وزن مولکولی پروتئین ها تکنیک SDS-PAGE (الکتروفورز ژل پلی اکریل آمید دودسیل سولفات سدیم) است. به دلیل استفاده از ماده سدیم دودسیل سولفات (SDS) و همچنین ویژگی های عالی ژل پلی اکریل آمید در تکنیک SDS-PAGE قدرت تفکیک پروتئین ها بسیار عالی می باشد. در تکنیک SDS-PAGE پروتئین هایی که الکتروفورز شده اند و براساس اندازه در ژل پلی اکریل آمید مرتب می شوند.
تاریخچه
در سال 1948، آرنه تیزلیوس با کشف الکتروفورز به عنوان متدی در مهاجرت اتمها یا مولکولهای باردار و محلول در میدان الکتریکی جایزه نوبل شیمی را دریافت کرد. استفاده از یک ماتریس جامد (در ابتدا دیسک های کاغذی) در الکتروفورز جداسازی را بهبود بخشید. الکتروفورز ناپیوسته در سال 1964 توسط L. Ornstein و B. J. Davis امکان بهبود جداسازی با اثر انباشتگی را فراهم کرد.
استفاده از هیدروژل های پلی اکریل آمید با پیوند متقابل، بر خلاف دیسک های کاغذی یا ژل های نشاسته ای که قبلا استفاده می شد، پایداری بالاتر ژل و عدم تجزیه میکروبی را فراهم کرد. اثر دناتوره کنندگی SDS در ژل های پلی اکریل آمید پیوسته و بهبود متعاقب آن در وضوح برای اولین بار در سال 1965 توسط دیوید اف سامرز در گروه کاری جیمز ای. دارنل برای جداسازی پروتئین های ویروس فلج اطفال توصیف شد. نوع فعلی تکنیک SDS-PAGE (الکتروفورز ژل سدیم دودسیل سولفات-پلی اکریل آمید) یک سیستم الکتروفورتیک ناپیوسته است در سال 1970 توسط Ulrich K. Laemmli توصیف شد و در ابتدا برای مشخص کردن پروتئین های سر باکتریوفاژ T4 استفاده شد.
تکنیک SDS-PAGE معمولاً به عنوان روشی برای جداسازی پروتئین هایی با جرم مولکولی بین 5 تا 250 کیلو دالتون استفاده می شود. استفاده ترکیبی از سدیم دودسیل سولفات (SDS، همچنین به عنوان سدیم لوریل سولفات نیز شناخته می شود) و ژل پلی اکریل آمید در اجازه می دهد تا تأثیر ساختار و بار را از بین ببریم و پروتئین ها تنها بر اساس تفاوت در وزن مولکولی آنها جدا شوند.
در تکنیک SDS-PAGE هنگامی که پروتئین ها از نمونه استخراج می شوند، روی ژل ساخته شده از SDS و پلی اکریل آمید اجرا می شوند. SDS یک ماده شوینده آنیونی است که برای خطی کردن پروتئین ها (پروتئین های دناتوره) و ایجاد بار منفی به پروتئین های خطی شده متناسب با جرم مولکولی آنها استفاده می شود.
پلی اکریل آمید به تکیه گاه جامد ژل تبدیل می شود. پروتئین های دناتوره شده که دارای بار منفی هستند از طریق ژل به سمت انتهای مثبت مهاجرت می کنند. با توجه به اندازه پروتئین ها، سرعت مهاجرت بین پروتئین ها متفاوت است و جداسازی اتفاق می افتد. بنابراین، تکنیک SDS-PAGE برای جداسازی تک تک پروتئین ها بر اساس اندازه آنها مفید و موثر است.
نکته: تکنیک SDS-PAGE یک محدودیت عمده در آنالیز پروتئین دارد. از آنجایی که SDS پروتئین ها را قبل از جداسازی دناتوره می کند، امکان تشخیص فعالیت آنزیمی، برهمکنش های اتصال پروتئین، کوفاکتورهای پروتئینی و غیره را نمی دهد.
همانطور که توضیح داده شد، تکنیک SDS-PAGE در حالی که یکی از دقیقترین و کمهزینهترین روشهای جداسازی و آنالیز پروتئین است، پروتئینها را دناتوره میکند. در مواردی که شرایط غیر دناتورهای ضروری است، پروتئینها با روشهای کروماتوگرافی متفاوت با کمیسنجی فتومتریک بعدی، برای مثال کروماتوگرافی میل ترکیبی (یا حتی خالصسازی میل ترکیبی پشت سر هم)، کروماتوگرافی حذف اندازه، کروماتوگرافی تبادل یونی جدا میشوند.
پروتئین ها را نیز می توان بر اساس اندازه در اولترافیلتراسیون جدا کرد. تک پروتئین ها را می توان با کروماتوگرافی میل ترکیبی یا با روش pull-down از یک مخلوط جدا کرد. برخی از روشهای جداسازی اولیه و مقرونبهصرفه، اما معمولاً مبتنی بر یک سری از استخراجها و رسوبگذاریها با استفاده از مولکولهای kosmotropic هستند، بهعنوان مثال، بارش سولفات آمونیوم و رسوب پلیاتیلن گلیکول.
تفاوت بین اکریل آمید و پلی اکریل آمید چیست؟
آکریل آمید: فرمول مولکولی آکریل آمید C3H5NO است.
پلی آکریل آمید: مولکول های پلی آکریل آمید از مولکول های آکریل آمید با پلیمریزاسیون به صورت خطی ساده یا به صورت اتصال عرضی تولید می شوند.
خواص اکریل آمید و پلی اکریل آمید:
اکریل آمید:اکریل آمید یک آمید کریستالی بسیار محلول در آب بی رنگ و بی بو است که می تواند به سرعت پلیمریزه شود و ترکیبات پلیمری را تشکیل دهد. این ماده به عنوان یک ماده سرطان زا، تحریک کننده پوست در نظر گرفته می شود و ممکن است یکی از عوامل ایجاد کننده سرطان پوست باشد.
پلی اکریل آمید: پلی آکریل آمید یک مولکول بسیار جاذب آب است و هنگامی که هیدراته می شود ژل نرمی تشکیل می دهد. این ویژگی در برخی کاربردهای صنعتی مانند ساخت لنزهای تماسی نرم دارای مزایای متعددی است.
موارد استفاده از اکریل آمید و پلی اکریل آمید:
آکریل آمید: آکریل آمید به مقدار زیاد برای تولید پلیمرهای مختلف استفاده می شود. علاوه بر این، از آن به عنوان عامل ضخیم کننده یا لخته ساز، لوازم آرایشی، تولید شکر، فرآوری سنگ معدن، بسته بندی مواد غذایی، جلوگیری از فرسایش خاک، تولید پلاستیک و کاغذ استفاده می شود. علاوه بر این، به عنوان یک واسطه شیمیایی در تولید N-methylol acrylamide و N-butoxyacry و همچنین در برخی از خاک های گلدان نیز استفاده می شود.
پلیاکریل آمید: پلی آکریل آمید عمدتاً برای لخته سازی جامدات در مایعات استفاده می شود. این فرآیند در تصفیه آب، کاغذسازی کاربرد دارد. یکی دیگر از کاربردهای پلی آکریل آمید استفاده به عنوان یک نرم کننده خاک است که اغلب در باغبانی و کشاورزی برای کنترل فرسایش خاک استفاده می شود. علاوه بر این، معمولاً در زمینه زیست شناسی مولکولی به عنوان محیطی برای الکتروفورز پروتئین ها و اسیدهای نوکلئیک استفاده می شود. اخیراً به عنوان فیلر زیر پوستی در جراحی های صورت شناسایی شده است. زنجیره مستقیم پلی آکریل آمید به عنوان ضخیم کننده و عامل تعلیق استفاده می شود. همچنین برای تولید لنزهای تماسی نرم استفاده می شود.
تهیه ژل پلی اکریل آمید برای تجزیه پروتئین ها یک مرحله مهم در تکنیک SDS- PAGE است. غلظت صحیح پلی اکریل آمید و نوع عامل اتصال متقابل استفاده شده به شدت بر خواص فیزیکی ژل تأثیر می گذارد که باعث جداسازی واقعی پروتئین های مختلف می شود. اندازه منافذ ژل برای جداسازی موثر باید به درستی مدیریت شود. با این حال، SDS- PAGE به عنوان یک تکنیک جداسازی پروتئین با وضوح بالا در نظر گرفته می شود.
تکنیک SDS-PAGE یک محدودیت عمده در آنالیز پروتئین دارد. از آنجایی که SDS پروتئین ها را قبل از جداسازی دناتوره می کند، امکان تشخیص فعالیت آنزیمی، برهمکنش های اتصال پروتئین، کوفاکتورهای پروتئینی و غیره را نمی دهد.
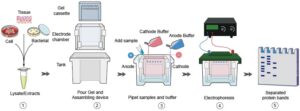
از این روش برای جداسازی مخلوط پروتئینهای حاصل از تجزیهی یک سلول میتوان استفاده نمود. در این روش در حضور سدیم دو دسیل سولفات (SDS)، به عنوان نوعی دترجنت، پروتئینها دناتوره میشوند. بعد از اضافه کردن SDS و احاطه شدن پروتئینها توسط آن، پروتئینها بار نسبتاً همسان پیدا کرده و به صورت خطی در میآیند؛ بدین ترتیب جداسازی فقط بر اساس اندازه صورت میپذیرد. تعداد مولکولهای SDS متناسب با تعداد آمینواسیدهای یک پروتئین است.
هر مولکول SDS دو بار منفی به پروتئین میدهد، همچنین باعث میشود که نیروهایی که در تا شدن و تغییر شکل دادن پروتئینها شرکت میکنند از بین بروند. در فرآیند الکتروفورز بر روی ژل پلی آکریل آمید، پروتئینها در یک میدان الکتریکی از سمت قطب منفی به سمت قطب مثبت حرکت میکنند و بر مبنای اختلاف در اندازه و بار الکتریکی از هم جدا میگردند. هر چه غلظت ژل بیشتر باشد، قطر منافذ ژل کوچکتر و حرکت پروتئینها در ژل کندتر میشود.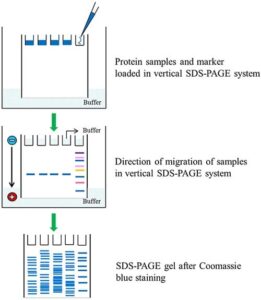
ژل به عنوان یک غربال عمل می کند که از طریق آن پروتئین ها در پاسخ به میدان الکتریکی حرکت می کنند. پروتئین ها دارای بار کلی مثبت یا منفی هستند. این حرکت یک مولکول پروتئین را به سمت نقطه ایزوالکتریک که در آن مولکول بار خالص ندارد، امکان پذیر می کند. با دناتوره کردن پروتئین ها و دادن بار منفی یکنواخت به آنها، می توان آنها را بر اساس اندازه در هنگام مهاجرت به سمت الکترود مثبت جدا کرد.
ژلهای با درصد بالای پلی آکریل آمید برای جداسازی پروتئینهای با وزن مولکولی کمتر مناسب هستند. علاوه بر قطر منافذ ژل، اندازه، شکل و بار پروتئینها نیز بر سرعت و میزان حرکت پروتئینها در بستر ژل در داخل میدان الکتریکی موثر است. بدون SDS، پروتئین با ساختمان اولیه خود و بدون تغییر بار جداسازی میشود، که در این روش جرم مولکولی و بار ایزوالکتریک در جداسازی تاثیر گذار بوده و این روش PAGE نام دارد.
در تکنیک SDS-PAGE از دو ژل مجزا استفاده میگردد؛
- ژل جدا کننده
- ژل متراکم کننده
ژل متراکم کننده بر روی ژل جدا کننده قرار میگیرد و چاهکهای لازم برای نمونهها در این بخش ایجاد میشوند. پس از رسیدن و جمع شدن نمونهها در حد فاصل دو ژل، پروتئینها وارد ژل جدا کننده شده و بر اساس تفاوت در اندازه از هم جدا می گردند.
افزودن 2-مرکاپتواتانول و یا دی تیوتریتول به بافر loading نمونهها باعث حذف پیوندهای دی سولفیدی و افزایش انحلال پذیری پروتئینهای نمونه میشود.
روش کار:
1 پیش از آغاز کار باید بافرها و محلولها ی زیر تهیه شوند؛
Tris.HCL با غلظت 5/1 مولار: 91 گرم Tris به منظور رسیدن به غلظت 5/1 مولار در آب دیونیزهی استریل حل شود و سپس pH در نقطهی 8/8 تنظیم شود. در ادامه با افزودن آب مقطر حجم محلول به 500 میلی لیتر رسانیده شود. برا ی تنظیم pH از هیدروکسید سدیم 1 نرمال و کلریدریک اسید 1 نرمال استفاده شود.
Tris.HCL با غلظت 1 مولار: 8/78 گرم Tris برای رسیدن به غلظت 1 مولار در 300 میلی لیتر آب مقطر دیونیزه حل شود و سپس pH سنجیده شد و در نقطهی 8/6 تنظیم گردد. در نهایت حجم محلول با آب مقطر به 500 میلی لیتر افزایش یابد.
سدیم دو دسیل سولفات %10: مقدار مناسبی از SDS برای رسیدن به غلظت (W/V) %10در آب مقطر دیونیزه حل گردد. محلول باید صاف و بیرنگ باشد.
آمونیوم پر سولفات %10: مقدار مناسبی از پودر APS برای رسیدن به غلظت (W/V) %10 در آب مقطر دیونیزه حل گردد.
ایزوبوتانول اشباع با آب: مقدار مناسبی از ایزوبوتانول با آب مقطر دیونیزه برای رسیدن به غلظت (V/V) %50 کاملاً مخلوط گردد. وقتی فالکون محتوی ایزوبوتانول اشباع شده با آب بی حرکت باشد، دو فاز تشکیل میگردد که فاز رویی ایزوبوتانول اشباع است و باید از آن استفاده کرد.
بافر Laemmli (2X): %20 گلیسرول، بافر Tris HCl 125/0 مولار، %10 2- مرکاپتواتانول، % 004/0 برمو فنل بلو، %4 SDS، 8/6= pH.
- صفحات شیشهای (spacer)، گیرهها و شانه مورد استفاده برای ایجاد چاهک شسته و با اتانول مطلق تمیز شوند.
- دو صفحهی شیشهای ما بین گیرهها قرار گرفته و بر روی دستگاه نگهدارنده ثابت شوند. سپس با استفاده از پیپت پاستور استریل، ژل جدا کننده ما بین دو صفحه جدا کننده ریخته شود.
| مواد مورد استفاده | حجم |
| پلی آکریل آمید 40 در صد | 3 میلی لیتر |
| Tris.HCL (5/1 مولار با 8/8 pH=) | 5/2 میلی لیتر |
| SDS 10% | 100 میکرولیتر |
| APS 10% | 100 میکرولیتر |
| TEMED | 5 میکرولیتر |
| آب مقطر دیونیزه | 32/4 میلی لیتر |
مواد مورد استفاده برای تهیهی ژل جدا کننده %12.
3- یک لایهی نازک از ایزوبوتانول اشباع شده با آب، بر روی سطح ژل جدا کننده ریخته شود تا سطح بالایی ژل در مجاورت اکسیژن هوا قرار نگیرد.
4- پس از پلیمریزه شدن ژل جدا کننده، ژل متراکم کنندهی 4 درصد طبق جدول زیر تهیه گردید:
| مواد مورد استفاده | حجم |
| پلی آکریل آمید 40 در صد | 1 میلی لیتر |
| Tris.HCL (1 مولار با 8/6 pH=) | 25/1 میلی لیتر |
| SDS 10% | 100 میکرولیتر |
| APS 10% | 100 میکرولیتر |
|
TEMED |
10 میکرولیتر |
| آب مقطر دیونیزه | 6/7 میلی لیتر |
مواد مورد استفاده برای تهیهی ژل متراکم کنندهی %4
- لایهی ایزوبوتانول از بین صفحات شیشهای خارج شود و روی ژل چند مرتبه با آب مقطر شسته شود.
- ژل متراکم کننده به آرامی و بدون ایجاد حباب در فضای بین دو شیشه بر روی ژل جدا کننده ریخته شود. شانه برای ایجاد چاهکها در داخل ژل متراکم کننده ما بین دو شیشه قرار داده شود.
- بافر Running به شکل زیر تهیه گردد:
- 3 گرم Tris، 4/14 گرم گلاسین و 1 گرم SDS در 800 میلی لیتر آب مقطر استریل حل شود و سپس حجم محلول با مقطر به 1000 میلی لیتر برسد.
- پس از پلیمریزه شدن ژل متراکم کننده شانه از فضای بین دو شیشه خارج گردد و شیشههای جداکننده در دستگاه الکتروفورز عمودی قرار داده شود.
- تانک الکتروفورز با بافر Running پر شود.
- مقدار 50 میلی گرم پروتئین از نمونههای مورد نظر با حجم مساوی از بافر (×2) Laemmli در میکروتیوبهایی مخلوط شده و به مدت 5 دقیقه در آب جوش، جوشانده شوند و در نهایت در چاهکهای ژل لود شوند. در کنار نمونهها مقدار 5 میکرولیتر از نشانگر پروتئین نیز در داخل یکی از چاهکها ریختهشود.
- برای عبور نمونهها از ژل متراکم کننده، ولتاژ دستگاه بر روی 60 ولت تنظیم شود.
- پس از عبور نمونهها از ژل بالایی و ورود آنها به ژل جدا کننده ولتاژ دستگاه به 120 ولت افزایش یابد.
- الکتروفورز تا مان رسیدن خط نشانهی آبی رنگ به انتهای ژل ادامه یابد و سپس دستگاه خاموش گردد (در حدود 90 دقیقه).
- ژل به آرامی از فضای بین دو شیشه خارج شود و از آن برای انجام وسترن بلاتینگ و رنگآمیزی پروتئینها با کوماسی بلو استفاده شود.
رنگآمیزی ژل پلی آکریل آمید با کوماسی بلو R-250
مواد و وسایل لازم:
کوماسی بریلیانت بلو R-250، متانول، استیک اسید، آب مقطر استریل، اتانول مطلق، shaker.
روش کار:
- 5/0 گرم کوماسی بلو در 90 میلی لیتر متانول، 20 میلی لیتر استیک اسید، 80 میلی لیتر آب مقطر حل شود و سپس به حجم نهایی 200 میلی لیتر رسانیده شود.
- ژل جداکننده در داخل ظرف استریلی که با اتانول مطلق شسته شده بود، قرار داده شود و محلول آمادهی کوماسی بلو روی ژل ریخته شود.
- ظرف حاوی ژل به صورت شبانه بر روی shaker قرار داده شود.
رنگبری ژل پلی آکریل آمید به منظور مشاهدهی باندهای پروتئین
مواد و وسایل لازم:
متانول، استیک اسید، آب مقطر استریل، shaker.
روش کار:
- 450 میلی لیتر متانول در 100 میلی لیتر استیک اسید حل شد و با 450 میلی لیتر به حجم یک لیتر برسد.
- رنگ کوماسی بلو از داخل ظرف خارج شد و 200 میلیلیتر از محلول رنگبری بر روی ژل ریخته شد و ظرف حاوی ژل روی shaker قرار داده برسد.
- در ابتدا که محلول رنگبری سریع آبی میشود باید در فواصل زمانی کوتاه محلول را با 200 میلی لیتر محلول تازه تعویض کرد.
- رنگبری ژل تا کمرنگ شدن رنگ آبی زمینهی ژل و ظاهر شدن باندهای پروتئینی باید ادامه یابد.
تفاوت SDS-PAGE و وسترن بلات:
پیش از پرداختن به تفاوت SDS-PAGE و وسترن بلات ابتدا باید بدانیم وسترن بلات چه تکنیکی است؟
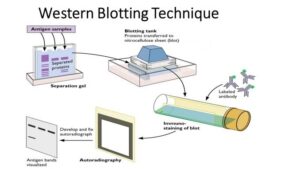
وسترن بلات یک تکنیک مهم در زیست شناسی سلولی و مولکولی است. با استفاده از وسترن بلات، محققان می توانند پروتئین های خاصی را از مخلوط پیچیده ای از پروتئین های استخراج شده از سلول ها شناسایی کنند. این تکنیک از سه عنصر برای انجام این کار استفاده می کند:
- جداسازی بر اساس اندازه
- انتقال به یک تکیه گاه جامد
- علامت گذاری پروتئین هدف با استفاده از یک آنتی بادی اولیه و ثانویه مناسب برای تجسم.
وسترن بلات (پروتئین بلاتینگ یا ایمنو بلاتینگ) اغلب در تحقیقات برای جداسازی و شناسایی پروتئین ها استفاده می شود. در این روش مخلوطی از پروتئین ها بر اساس وزن مولکولی و در نتیجه بر اساس نوع، از طریق الکتروفورز ژل جدا می شود. این نتایج سپس به غشایی که نواری برای هر پروتئین تولید می کند، منتقل می شود. سپس غشاء با برچسب آنتی بادی های مخصوص پروتئین مورد نظر انکوبه می شود.
یا به عبارت دیگر؛ وسترن بلات روشی است که در طی فرآیند بلاتینگ برای به دست آوردن تصویر آینه ای از الگوهای پروتئین در ژل پلی اکریل آمید SDS استفاده می شود. غشایی که برای وسترن بلات استفاده می شود بیشتر از نیتروسلولز یا پلی وینیلیدین دی فلوراید (PVDF) تشکیل شده است. غشا با پروتئین منتقل شده می تواند برای شناسایی پروتئین مورد نظر استفاده شود. برای تشخیص پروتئین مورد نظر با هیبریداسیون به آنتی بادی با کیفیت بالا نیاز دارد. آنتی بادی به آنتی ژن اختصاصی خود متصل می شود و وجود آنتی ژن مورد نظر که یک پروتئین است را آشکار می کند.
آنتی بادی غیر متصل شسته می شود و تنها آنتی بادی متصل به پروتئین مورد نظر باقی می ماند. سپس آنتی بادی های متصل شده با ایجاد فیلم شناسایی می شوند. از آنجایی که آنتی بادی ها فقط به پروتئین مورد نظر متصل می شوند، تنها یک نوار باید قابل مشاهده باشد. ضخامت نوار مربوط به مقدار پروتئین موجود است. بنابراین انجام یک استاندارد می تواند میزان پروتئین موجود را نشان دهد.
در واقع تکنیک SDS-PAGE و وسترن بلات دو تکنیک در آنالیز پروتئین ها هستند. تکنیک SDS-PAGE امکان جداسازی آسان پروتئین ها را بر روی ژل با توجه به وزن مولکولی آنها فراهم می کند. وسترن بلات به تأیید وجود و کمیت یک پروتئین خاص از طریق هیبریداسیون با آنتی بادی های خاص کمک می کند. این تفاوت تکنیک SDS-PAGE و وسترن بلات است.
انتقال پروتئین از ژل پلی اکریل آمید SDS به وسترن بلات با الکتروبلات انجام می شود. این یک روش موثر و سریع است که باعث می شود پروتئین ها از ژل الکتروفورز شده و به غشای نیتروسلولزی (Western blot) منتقل شوند.
تکنیک SDS-PAGE (الکتروفورز ژل پلی آکریل آمید سدیم دودسیل سولفات) نوعی روش الکتروفورز ژل است که برای جداسازی پروتئین ها بر اساس اندازه آنها (وزن مولکولی) استفاده می شود. وسترن بلات یک صفحه مخصوص از یک غشای بلاتینگ است که برای انتقال همان الگوی پروتئین ها در تکنیک SDS-PAGE استفاده می شود. تفاوت اصلی بین تکنیک SDS-PAGE و وسترن بلات در این است که تکنیک SDS-PAGE به جداسازی پروتئین ها در یک مخلوط اجازه می دهد در حالی که وسترن بلات امکان تشخیص و تعیین کمیت یک پروتئین خاص از یک مخلوط را فراهم می کند. هر دو تکنیک SDS-PAGE و وسترن بلات در مطالعات آنالیز پروتئین مفید هستند.









































