تکنیک های نوترکیبی برای تشخیص ژن های مسئول بیماری های ارثی و طراحی روش های درمانی جدید برای این اختلالات، استفاده از ژن های کلون شده برای تولید داروهای نوترکیب و واکسن
پزشکی یک شاخه ذینفع مهم ازانقلاب نوترکیبی DNA بوده است و خواهد بود، به طوری که می توان یک کتاب کامل را درمورد این موضوع نوشت. درادامه مطلب می بینیم که چگونه از تکنیک های نوترکیبی DNA برای تشخیص ژن های مسئول بیماری های ارثی وطراحی روش های درمانی جدید برای این اختلالات، استفاده می شود. در ابتدا روش هایی را که درآن ژن های کلون شده برای تولید داروهای نوترکیب به کار می روند، بررسی می کنیم.

کلونینگ ژن؛ تولید داروهای نوترکیب
ریشه ی بسیاری از بیماری های انسانی فقدان یا اختلال در عملکرد یک پروتئین است که به طور طبیعی در بدن ساخته نمی شود. اکثر این بیماری ها را می توان با تجویز شکل طبیعی پروتئین به بیمار درمان کرد، اما برای اینکه این روش درمانی امکان پذیر باشد، باید شکل طبیعی پروتئین مورد نظر در مقیاس بالایی در دسترس باشد.
اگر این نقص به کمک تجویز پروتئین های انسانی تصحیح شود، آنگاه بدست آوردن مقادیر کافی از پروتئین مورد نظر، یک مشکل بزرگ خواهد بود، مگر اینکه از خون اهدایی به عنوان منبع پروتئین استفاده کنیم. بنابراین از پروتئین های حیوانی در هر مورد که موثر باشند می توان استفاده کرد. اما تعداد بیماری هایی که با پروتئین حیوانی درمان می شوند، خیلی زیاد نیست و همچنین همیشه امکان بروز عوارض جانبی مانند پاسخ آلرژیک در اثر مصرف پروتئین های حیوانی وجود دارد.
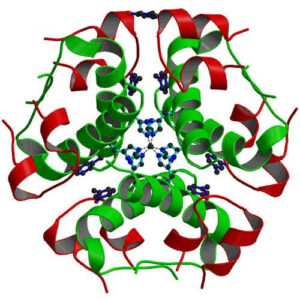 کلونینگ ژن؛ انسولین نوترکیب
کلونینگ ژن؛ انسولین نوترکیب
انسولین که توسط سلول های β جزایر لانگرهانس پانکراس ساخته می شود، سطح گلوکز را در خون کنترل می کند. نقص در انسولین باعث بروز دیابت ملیتوس می شود، که مجموعه ای از علائمی ست که اگر درمان نشود، منجر به مرگ بیمار می شود .
انسولین دارای دو ویژگی است که سبب تسهیل تولید آن از طریق تکنولوژی DNA نوترکیب می شود:
- انسولین انسانی بعد از ترجمه دچار هیچ تغییری مانند اضافه کردن ریشه قندی نمی شود، بنابراین امکان ساخته شدن انسولین توسط باکتری ها وجود دارد.
- اندازه مولکولی انسولین که یک پروتئین کوچک است و شامل دو پلی پپتید است.
- در انسان این زنجیرها بصورت یک پیش سازه پره پروانسولین ساخته می شود که شامل قطعات A و B است که توسط یک زنجیره ی دیگر(زنجیره C) به هم وصل شده اند و در ابتدای این پیش ساز هم یک توالی وجود دارد. بعد از ترجمه توالی پیشرو حذف می شود و زنجیره ی C نیز برش می خورد و در نهایت پلی پپتیدهای A و B باقی می مانند که بوسیله ی دو باند دی سولفیدی به هم متصل شده اند.
- چندین استراتژی برای بدست آوردن انسولین نوترکیب به کار بسته شده است. اولین پروژه شامل ساخت ژن های مصنوعی زنجیره های A و B و اتصال دو زنجیره در سلول E.coli بود که این کار همان تکنیک های عمومی به کار رفته در تولید پروتئین نوترکیب است.
فرآیند ساخت انسولین نوترکیب از ژن های مصنوعی زنجیر برای ساخت و بیان ژن های مصنوعی انسولین
در اواخر دهه ی 1970، ایده ی ساخت یک ژن مصنوعی بسیار نوآورانه بود. در آن زمان ساخت الیگونوکلئوتیدها در دوران ابتدایی خویش به سر می برد و روش های در دسترسی که با آنها بتوان مولکول های DNA مصنوعی را بسازیم بسیار مشکل تر از تکنیک های اتوماتیک امروزی بود. با این وجود، ژنی که زنجیره های A وb انسولین را کد کند، در سال 1978 ساخته شد.
در این فرایند توالی های سه نوکلئوتیدی ساخته شد که نماینده ی همه ی کدون های ممکن بودند و این توالی ها بر اساس زنجیره های A و B به هم متصل شدند. این ژن مصنوعی لزوماً دارای همان توالی نوکلئوتیدی ژن های واقعی زنجیره های A وb نبود، اما توانست باعث تولید پلی پپتید صحیح شود. دو پلاسمید نوترکیب یکی حامل ژن مصنوعی زنجیره ی A و یکی حامل زنجیره ی B ساخته شد.
ژن مصنوعی، هر زنجیره را به یک قالب باز خواندن LacZ’ در وکتور Pbr322 متصل کردند. بنابراین ژن انسولین، تحت کنترل پروموتر قوی Lac قرار می گرفت و درنتیجه ژن به صورت یک پروتئین همجوش بیان می شد که شامل چند اسیدآمینه ی اول ژن بتاگالاکتوزیداز و پلی پپتیدهای A و b بود.
هر ژن طوری طراحی شده بود که بین قسمت بتاگالاکتوزیداز و قسمت انسولین یک زائده ی متیونین قرار بگیرد که بدین وسیله پلی پپتید انسولین را بتوان از قطعه ی بتاگالاکتوزیداز به کمک آنزیم سیانوژن برمید برش داد. سپس زنجیره های A و B را تخلیص کرده و در آزمایشگاه از طریق باند دی سولفیدی به هم متصل کردند. مرحله ی نهایی یعنی تشکیل باندهای دی سولفیدی نسبتاً ناکارآمد است.
در یک روش پیشرفته تر محققین چارچوب کامل خواندن پره انسولین که شامل زنجیره ی A، زنجیره ی C و زنجیره ی B بود را ساختند. گرچه ساختن DNA به این روش بسیار سخت تر است اما دارای این مزیت خواهد بود که در آن پره هورمون به طور خودبه خود دچار تاخوردگی می شود و ساختار باندهای دی سولفیدی صحیح خود را بدست می آورد. زنجیره های C را هم در نهایت می توان با یک برش پروتئولیتیک جدا کرد.
سنتز هورمون های رشد انسانی در E.coli
همان زمانی که انسولین نوترکیب برای اولین بار در E.coli ساخته شد، دانشمندان دیگری روی پروژه ای مشابه برای تولید هورمون رشد سوماتواستاتین و سوماتوتروپین، مطالعه می کردند. این دو پروتئین به همراه هم در کنترل پروسه ی رشد بدن انسان دخالت دارند و نقص در عملکرد آنها منجر به اختلالات دردناک و ناتوان کننده ای مانند آکرومگالی (رشد کنترل نشده ی استخوان) و کوتولگی می شود.
سوماتواستاتین اولین پروتئین انسانی بود که در E.coli تولید شد. این پروتئین به خاطر اینکه بسیار کوچک است و فقط 14 اسیدآمینه دارد، ساخت ژن مصنوعی آن بسیار آسان است.
استراتژی که برای ساخت آن استفاده شد شبیه همان بود که برای تولید انسولین نوترکیب استفاده شد، یعنی داخل کردن ژن مصنوعی درون وکتور LacZ’ و ساخت یک پروتئین همجوش و سپس برش آن به وسیله ی سیانوژن برمید. ساختن سوماتوتروپین کمی مشکل تر بود زیرا این پروتئین دارای 191 اسیدآمینه است که معادل تقریباً 600 جفت باز خواهد بود.
بنابراین ساخت این DNA در اواخر دهه ی 1970 تقریباً غیرممکن به نظر می رسید. برای ساخت سوماتوتروپین نوترکیب از مجموعه ای از روش های ساخت ژن مصنوعی و کلونینگ DNA مکمل استفاده شد تا سویه ای از E.coli تولید کننده ی سوماتوتروپین بدست آید.
mRNA از هیپوفیز(غده ای که سوماتوتروپین را در بدن تولید می کند) استخراج شد و کتابخانه ی cDNA سوماتوتروپین دارای یک جایگاه آنزیم محدودالاثر Hae III که می توانست cDNA را به دو قسمت برش دهد. قسمت بزرگ تر شامل کدون های 24 تا 191 بود که برای ساخت پلاسمید نوترکیب استفاده می شد و قسمت کوچکتر توسط یک مولکول DNA مصنوعی جایگزین شد که شامل ناحیه ی شروع ژن سوماتوتروپین بود و باعث فراهم شدن یک سیگنال صحیح برای ترجمه در E.coli می شد و سپس ژن تغییریافته را وارد یک وکتور بیانی کردندکه حامل پروموتر Lac بود.
پروتئین های نوترکیب انسانی و تولید واکسن های نوترکیب پروتئینی
فاکتور VIIIنوترکیب
گرچه بسیاری از ترکیبات دارویی از کلونینگ ژن ها در E.coli بدست آمده اند اما به دلیل مشکلی که در ارتباط با تولید بعضی پروتئین های خارجی در E.coli وجود داشت، سلول های یوکاریوت را با این ارگانیسم میزبان جایگزین کردند. یک نمونه ی تولید داروهای نوترکیب در سلول های یوکاریوت، فاکتور VIII انسانی می باشد. این پروتئین نقشی کلیدی در فرآیند لخته شدن خون دارد. شایع ترین نوع بیماری هموفیلی در انسان ناشی از ناکارایی بدن در تولید همین پروتئین است که منجر به اختلال در مسیر لخته شدن خون و بروز علائم شناخته شده ی این بیماری می شود.
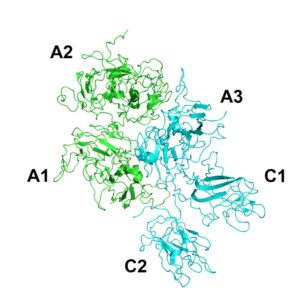
در گذشته ای نه چندان دور تنها راه درمان هموفیلی، تزریق فاکتور VIII تخلیص شده ای بود که از خون اهداکننده ها تهیه می شد. تخلیص فاکتور VIII یک فرآیند پیچیده و درمان با آن پرهزینه است و نکته ی مهم تری که بر سختی این روش می افزود تلاش برای حذف ذرات ویروسی بود که ممکن بود در خون وجود داشته باشد. هپاتیت و سندرم نقص ایمنی اکتسابی(ایدز) می تواند از طریق تزریق فاکتور VIII به بیماران هموفیلی انتقال یابد و در واقعیت هم این اتفاق افتاده است. تولید فاکتور VIII نوترکیب که عاری از این مشکلات آلودگی است، یک موفقیت چشم گیر در عرصه ی بیوتکنولوژی بوده است.
ژن فاکتور VIII بسیار بزرگ است و بیش از 186 کیلوباز طول دارد و دارای 26 اگزون و 25 اینترون می باشد. mRNA آن پلی پپتید بزرگی به طول 2351 اسیدآمینه را کد می کند که تحت فرآیندهای پیچیده ی بعد از ترجمه قرار می گیرد و در نهایت یک پروتئین دایمر شامل یک زیرواحد بزرگ مشتق شده از فرادست پلی پپتید اولیه و یک ساب یونیت کوچک که از فرودست آن مشتق شده است، تشکیل می شود.
دو ساب یونیت در کل شامل 17 باند دی سولفیدی و تعدادی جایگاه گلیکوزیله می باشند. پیش بینی ساخت فرم فعال چنین پروتئین بزرگ و پیچیده ای در E.coli غیرممکن است. بنابراین از همان ابتدا برای بدست آوردن فاکتور VIII نوترکیب، روی سلول های پستاندار تلاش می کردند. در اولین آزمایش کل cDNA در سلول هامستر کلون شد اما متاسفانه بازده پروتئینی بسیار پایینی داشت که احتمالاً به این خاطر بود که وقایع پس از ترجمه در سلول هامستر با اینکه به طور صحیح انجام می گرفت اما همه ی محصولات اولیه به فرم فعال تبدیل نمی شوند و در نهایت باعث کاهش مقدار محصول نهایی می شد.
در یک روش دیگر از دو قطعه ی جدای cDNA استفاده شد که یکی ساب یونیت بزرگ تر و یکی ساب یونیت کوچکتر را کد می کرد. هر قطعه ی cDNAدرون یک وکتور بیانی در پایین دست پروموتر Ag و بالادست سیگنال پلی آدنیلاسیون ویروس SV40وارد شد. پلاسمیدها را وارد سلول های هامستر کردند و پروتئین نوترکیب مورد نظر بدست آمد. بازده پروتئینی در این روش، ده برابر بیشتر از روشی بود که سلول حاوی cDNAکامل بود و همچنین پروتئین بدست آمده از نظر عملکردی از فرم طبیعی آن غیر قابل تمایز بود.
از فارمینگ هم برای تولید فاکتور هشت استفاده کردند. cDNA کامل انسانی را به پروموتر ژن پروتئین اسیدی آب پنیر خوک متصل کردند تا این پروتئین در بافت پستان خوک سنتز شود و متعاقباً منجر به ترشح آن در شیر حیوان شود. فاکتور هشتی که با استفاده این روش تولید شد دقیقاً مشابه همان پروتئین طبیعی انسان بود و عملکرد کاملی را در روند لخته شدن خون از خود نشان می داد.
سنتز سایر پروتئین های نوترکیب انسانی
شمار پروتئین های انسانی که بوسیله تکنولوژی نوترکیبی ساخته می شوند همچنان در حال افزایش است. این تکنولوژی علاوه بر اینکه با تولید پروتئین هایی به منظور جایگزینی پروتئین های دارای نقص عملکردی و یا تامین کمبود آنها، باعث درمان خیلی از بیماری ها شده است، همچنین تعدادی از فاکتورهای رشد مانند اینترفرون ها و اینترکولین ها که در درمان سرطان قابل استفاده اند را نیز تولید کرده است.
از آنجایی که این پروتئین ها به مقدار بسیار کمی در بدن انسان ساخته می شوند، بنابراین تنها راه بدست آوردن این پروتئین ها با مقادیر بالا برای اهداف بالینی، تکنولوژی نوترکیبی می باشد. سایر پروتئین ها بسیار آسان تر بدست می آیند(مانند آلبومین)، اما از آنجا که به مقادیر زیادی از آنها نیاز است، تولید آنها هم در میکروارگانیسم ها یک گزینه مورد توجه خواهد بود.
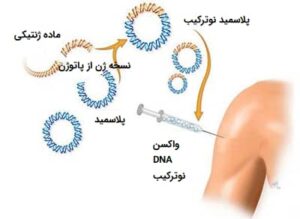
واکسن های نوترکیب
واکسن یک فرآورده ی آنتی ژنی است که بعد از تزریق به جریان خون سیستم ایمنی بدن را تحریک می کند تا با تولید آنتی بادی بدن را در مقابل عفونت محافظت کند. ماده ی آنتی ژنیکی که در واکسن وجود دارد، به طور معمول فرم غیرفعال شده عامل بیماری زاست. به طور مثال، واکسنهای ضد ویروسی، اغلب شامل ذرات ویروسی هستند که به وسیله ی حرارت یا یک روش مشابه تضعیف شده اند. در گذشته دو مشکل مانع تولید واکسن های تضعیف شده می شد:
* فرآیند غیرفعال سازی باید صد در صد کارآمد باشد زیرا حتی یک ذره ی ویروسی زنده در واکسن می تواند منجر به عفونت شود. این مسئله برای تولید واکسن های بیماری پا و دهان رخ داده بود.
* مقدار زیاد ذره های ویروسی که برای تولید واکسن نیاز هستند معمولاً از کشت بافت به دست می آمدند و متاسفانه بعضی از ویروس ها بخصوص ویروس هپاتیت Bدر کشت بافت رشد نمی کنند.
تولید واکسن بصورت پروتئین های نوترکیب
تاکید فرآیند کلونینگ ژن ها برای تولید واکسن نوترکیب روی این موضوع می باشد که آنتی بادی های اختصاصی ضد ویروس ها علاوه بر اینکه علیه ذرات ویروسی کامل تولید می شوند، می توانند فقط در مواجهه با قسمت جداشده ی خاصی از ویروس نیز تولید شوند. این موضوع بالاخص در مورد پروتئین های تخلیص شده ای که در پوشش ویروس حضور دارند، صدق می کند.
اگر ژن کد کننده ی پروتئین های آنتی ژنیک یک ویروس خاص شناسایی شود و آن را وارد یک وکتور بیانی کنند، بنابراین همان روشی که برای تولید پروتئین های حیوانی استفاده می شد این بار می تواند برای تولید پروتئین های نوترکیبی به کار رود که به عنوان واکسن استفاده شوند. مزیت این واکسن ها این است که ذره ی ویروسی کامل در آن وجود ندارد و همچنین می توانند در مقادیر بالا تولید شوند.
بزرگترین دستاورد استفاده از این روش تولید واکسن هپاتیت B بوده است. این ویروش در بسیاری از نقاط گرمسیر جهان اندمیک است و منجر به بیماری کبدی شده که بعد از یک دوره ی مزمن می تواند منجر به سرطان کبد شود. فردی که از بیماری هپاتیت B بهبود یافته است، در مقابل عفونت دوباره مصون خواهد بود. زیرا خون او حاوی آنتی بادی علیه پروتئین های سطحی پوشش ویروس هپاتیت B (HbsAg) است. این پروتئین در هر دو میزبان ساکارومایسس سرویزیه با استفاده پلاسمید دو میکرومتری و رده های سلولی تخمدان همستر چینی (CHO)، سنتز شده است. در هر دو مورد پروتئین در مقادیر بالایی تولید شده و تزریق آن به حیوان آزمایشگاهی باعث مصونیت در برابر بیماری هپاتیت B شده است.
نکته کلیدی در موفقیت واکسن HbsAg نوترکیب، به خاطر ویژگی غیر معمول عفونت زایی ویروس است. خون افراد مبتلا نه تنها حاوی ذرات ویروسی کامل هپاتیت B با قطر ۴۲ نانومتر است بلکه حاوی ذرات کروی ۲۲ نانومتری هم می باشد که فقط از پروتئین HbsAg تشکیل شده است. این ذرات ۲۲ نانومتری در مخمر و سلول CHOهم تشکیل می شوند و در واقع همین ذرات هستند که ماده ی موثر واکسن های نوترکیب را تشکیل می دهند.
بنابراین این واکسن های نوترکیب بخشی از پروسه ی عفونت طبیعی را تقلید می کنند و تولید آنتی بادی را در بدن تحریک می کندند، اما چون این ذرات کروی، ویروس های زنده نیستند، باعث بیماری نمی شوند. هر دو واکسن یوکاریوتی و مخمری برای انسان تایید شده است و سازمان بهداشت جهانی ارتقای استفاده ار آن را در برنامه ی واکسیناسیون ملی تایید کرده است.
همچنین واکسن های نوترکیب در مورد پاپیلوماویروس انسانی (HPV) با موفقیت ساخته شده اند که ساب تایپ های مختلف آن انواعی از سرطان ها را ایجاد می کنند. پروتئین پوششی L1در مخمر ساکارومایسس سرویسیه بیان شده است و باعث افزایش ذرات شبه ویروسی که تجمعی از پروتئین های L1 می باشند، شده است. دقیقا مشابه HbsAg این ذرات فاقد اسید نوکلئیک بوده و در نتیجه عفونت زا نمی باشند.
به منظور افزایش سطح تاثیر واکسن HPV نوترکیب، انواعی از سویه های مخمر نوترکیب تولید شدند که هر کدام پروتئین L1 از ساب تایپ مختلفی از HPV را سنتز می کردند. سپس این ذرات شبه ویروسی از سویه ها ترکیب شدند تا واکسنی دو ظرفیتی یا چهار ظرفیتی ایجاد کنند. این واکسن ها در بانوان در برابر ابتلا به سرطان دهانه رحم و از آقایان در برابر عفونت منتقله از طریق مقاربت محافظت می کنند.

واکسن های نوترکیب در گیاهان تراریخته
ظهور فارمینگ امکان استفاده از گیاهان تراریخته را به عنوان میزبانی برای ساخت واکسن های نوترکیب فراهم کرده است. سهولت رشد و کشت گیاهان به این معنی است که این تکنولوژی در کشورهای در حال توسعه قابل استفاده خواهد بود. زیرا در این کشورها هزینه ی بالای تولید پروتئین نوترکیب به مانعی برای تولید آن ها تبدیل شده است.
اگر تجویز واکسن نوترکیب به صورت خوراکی موثر واقع شود، بنابراین با خوردن تمام یا بخشی از گیاه مورد نظر، ایمنی مورد نظر حاصل می شود. تصور اینکه برای انجام یک برنامه ی گسترده ی واکسیناسیون روشی راحت تر و ارزان تر از این پیدا شود، دور از ذهن خواهد بود.
برای اثبات امکان پذیر بودن این روش از واکسن هایی مثل HbsAg و پروتئین های پوششی ویروس سرخک و ویروس سنسیشیال تنفسی به عنوان نمونه استفاده کردند. در هر سه مورد ایمنی مورد نظر در اثر تغذیه ی حیوانات آزمایشگاهی با این گیاهان تراریخته، حاصل شده است. تلاش هایی همچنین برای ساخت گیاهان تراریخته ای که چند نوع از واکسن را بیان کنند، انجام شده است که باعث ایجاد ایمنی علیه طیفی از بیماری ها فقط با خوردن یک گیاه شده است.
مشکل اصلی که کارخانه ها با آن مواجه اند، این است که مقدار پروتئین نوترکیبی که این گیاهان سنتز می کنند، اغلب کمتر از آن است که یک مصونیت کامل را علیه بیماری مورد نظر ایجاد کند. برای اثر بخشی کامل واکسن بازده ی آن باید شامل 10-8 تا درصد محتوای پروتئینی محلول در آن بخش از گیاه باشد که خورده می شود، اما در عمل بازده ی آن بسیار کمتر از این مقدار است و معمولا به بیش از نیم درصد نمی رسد.
تفاوت مقدار بازده در بین گیاهان مختلف هم یک مشکل دیگر است. یکی از کارهایی که برای حل مشکل می توان انجام داد این است که ژن کلون شده را به جای اینکه در هسته ی گیاه قرار دهیم، وارد ژنوم کلروپلاست آن کنیم. با این کار تولید پروتئین نوترکیب در گیاه بسیار بیشتر خواهد شد.
واکسن های مختلفی از طریق سنتز در کلروپلاست ایجاد شده اند که شامل واکسن ضد سیاه زخم، طاعون، آبله و انگل آنتاموبا هیستولیتکا می باشند. همچنین از کلروپلاست تنباکو و کاهو به منظور ساخت ترکیبی از پروتئین های پوششی Vibrio cholerae و Plasmodium falciparum استفاده شده است.
وقتی این گیاهان توسط موش خورده شدند، در برابر کلرا توکسین محافظت ایجاد کردند و همچنین باعث ساخت آنتی بادی شد که توانایی انگل های P.falciparum را برای تهاجم به سلول های قرمز خون کاهش می دهند (تاثیر این گیاهان در برابر مالاریا مستقیما قابل آزمایش در موش ها نمی باشند زیرا P.falciparum موش را آلوده نمی کند).
وبا و مالاریا از جمله بیماری های مهمی در بسیاری از نقاط جهان می باشد و ایجاد واکسنی که آسان تجویز شود و در عین حال محافظت دوگانه ایجاد کند پیشرفت بزرگی برای سلامتی انسان خواهد بود. گیاهان همچنین می توانند به روش کاملا متفاوتی علیه بیماری محافظت ایجاد کنند، زمانی که هدف ایجاد یک پروتئین که پاسخ ایمنی را تحریک کند نباشد، بلکه استفاده از گیاه به منظور ساخت آنتی بادی مخصوص آنتی ژن پروتئین پوششی A از Streptpcoccus mutans را کد می کنند.
بعد از دورگه سازی بین این رده ها، یک نوع از تنباکو ترانس ژن بدست آمد که حاوی هر چهار ژن کلون شده بود. سنتز آنتی بادی های دارای عملکرد توسط گیاهان، باعث تجمع آن ها در سلول های گیاهی می شود. S.mutans ساکن حفره دهانی انسان می باشد و علت اصلی پوسیدگی های دندانی است که بیش از 60 درصد کودکان را در کشورهای صنعتی در گیر می کند. یک منبع ارزان آنتی بادی هایی که بتوانند در برابر پوسیدگی دندانی محافظت ایجاد کنند و در عین حال به جای تزریق به صورت ساییدن رو سطح دندان ها تجویز شوند، برای سال های زیادی مورد جستجو بوده است.
واکسن های ویروسی زنده و افزایش کارایی سیستم ایمنی بدن
تاریخچه استفاده از ویروس واکسینا به عنوان واکسنی برای آبله به سال 1976 برمی گردد، زمانی که ادوارو جنر برای اولین بار متوجه شد، این ویروس که برای انسان بی خطر است می تواند سیستم ایمنی بدن را علیه یک ویروس بسیار خطرناک تر به نام ویروس آبله ی انسانی تحریک کند. ریشه لغت واکسن به کلمه ی واکسینیا برمی گردد که استفاده از آن منجر به ریشه کنی جهانی بیماری آبله در سال 1980 گردید.
یک ایده ی جدید این است که بتوان از ویروس واکسینیای نوترکیب به عنوان یک واکسن زنده علیه بیماری های دیگر استفاده کرد. اگر یک ژن کد کننده پروتئین پوششی ویروس به طور مثال HbsAg را وارد ژنوم واکسینیا کنیم، طوری که تحت کنترل پروموتر واکسینیا باشد این ژن بیان خواهد شد. بعد از تزریق به جریان خون، همانند سازی ویروس نوترکیب نه تنها ذرات ویروسی را زیاد می کند بلکه آنتی ژن سطحی هم به مقدار قابل توجهی افزایش خواهد یافت. بنابراین با این روش مصونیت علیه هم هپاتیت B و هم آبله انسانی حاصل می شود.
در این تکنیک توانایی بالقوه ی قابل توجهی نهفته است. ویروس های واکسینیای نوترکیب برای ژن های خارجی زیادی ساخته شده اند و باعث مصونیت در برابر آن بیماری خاص در حیوانات آزمایشگاهی شده اند. با مشخص شدن اینکه یک ویروس واکسینیای نوترکیب هر سه ژن هماگلوتینین ویروس آنفولانزا، HbsAg و گلیکوپروتئین ویروس هرپس سیمپلکس، توانسته در برابر هر سه بیماری در میمون مصونیت ایجاد کند، امکان ساخت واکسن های وسیع الطیف بیش از پیش مشخص شده است.
مطالعات نشان داده است که واکسیناسیون حیوانات با ویروس واکسینیایی که دارای ژن گلیکوپروتئین هاری است و ژن آنزیم تیمیدین کیناز آن حذف شده است، باعث مصونیت در برابر بیماری خواهد شد در حالی که حیوان به بیماری آبله گاوی که توسط خود ویروس واکسینیا ایجاد می شود مبتلا نمی شود. زیرا با حذف ژن تیمیدین کیناز امکان تکثیر ویروس از بین می رود. از این نوع واکسن ویروسی خاص هم اکنون در اروپا و امریکای شمالی برای کنترل هاری استفاده می شود.
تشخیص ژن هایی که مسئول بیماری های انسانی هستند
دومین زمینه قابل توجه تحقیقات پزشکی که در آن از کلونینگ ژن ها می توان استفاده کرد، تشخیص و جداسازی ژن های مسئول بیماری های انسانی است. یک بیماری ژنتیکی یا وراثتی، بیماری است که در اثر نقض در یک ژن خاص به وجود می آید. افرادی که حامل این ژن معیوب هستند، مستعد ابتلا به آن بیماری خاص در مرحله ای از زندگی خود هستند.
در بیماری های وراثتی که ژن مورد نظر روی کروموزوم X است (مانند هموفیلی) همه مردانی که دارای این ژن معیوب باشند این بیماری را بروز می دهند و زنانی که دارای یک ژن سالم و یک ژن معیوب هستند، بیمار نمی شوند.
اما می توانند این ژن معیوب را به فرزندان پسر خود منتقل کنند. سایر بیماری هایی که ژن معیوب مربوط به آن ها روی کروموزوم اتوزومال است، در اکثر موارد مغلوب هستند. بدین معنی که هر دو کروموزوم همتا باید دارای ژن معیوب باشند تا بیماری رخ دهد. تعداد کمی از بیماری ها مانند هانتینگتون، اتوزوم غالب هستند و بنابراین وجود فقط یک ژن ناقص روی یکی از جفت کروموزوم همتا، منجر به بیماری می شود.
در بعضی بیماری های ژنتیکی، علائم از همان آغاز تولد بروز کرده و در بعضی دیگر تا سنین بلوغ یا پیری بروز نخواهد کرد. سیستیک فیبروزیس مثالی از بیماری هایی است که از ابتدا زندگی بروز کرده و آلزایمر و هانتینگتون نمونه ای از بیماری هایی هستند که در میانسالی و پیری خود را نشان می دهند.
در تعدادی از بیماری ها مانند سرطان که به نظر می رسد زمینه ژنتیکی هم داشته باشند علائم پیچیده بیماری تا زمانی که توسط عوامی محیطی محرک و متابولیکی تحریک نشده اند، نهفته باقی می مانند. بنابراین اگر استعداد ابتلا به این بیماری در فردی تشخیص داده شود، می توان با مدیریت شیوه زندگی فرد احتمال بروز بیماری را کاهش داد.
بیماری های ژنتیکی همیشه در جوامع انسانی وجود داشته است اما اهمیت آن ها در سال های اخیر افزایش یافته است. دلیلش این است که برنامه های واکسیناسیون، آنتی بیوتیک ها و بهبود سطح بهداشت شیوع بیماری های عفونی مانند آبله، سل و وبا را که در اواسط قرن بیستم مهم ترین عامل مرگ ومیر بوده اند کاهش داده است. در نتیجه بخش بزرگی از جوامع انسانی امروزی در اثر بیماری های ژنتیکی می میرند. بویژه دلیل افزایش طول عمر انسان ها، بیماری هایی که در سال های آخر عمر بروز می کنند بسیار شایع شده اند.
به سه دلیل تشخیص بیماری های ژنتیکی مهم و ضروریست:
1- شناسایی ژن ممکن است منجر به فهمیدن اصول بیوشیمیایی بیماری شود و بدین ترتیب طراحی یک روش درمانی را ممکن می سازد.
2- با شناسایی موتاسیونی که در ژن معیوب رخ داده می توان برنامه های غربالگری را طراحی کرد که در آن ژن های موتاسیون یافته در افراد حامل که هنوز بیماری در آن ها بروز نکرده، تشخیص داده شود. افراد حامل می توانند با مشاوره ژنتیک، احتمال ابتلا به بیماری فرزندانشان را دریابند. تشخیص زودرس بیماری در افرادی که هنوز علائم بیماری در آن ها بروز نکرده است می تواند به آن ها کمک کند تا مراقبت های مورد نیاز را برای کاهش خطرات بیماری، اتخاذ کنند.
3-شناسایی ژن، پیش نیاز ژن درمانی است.










































