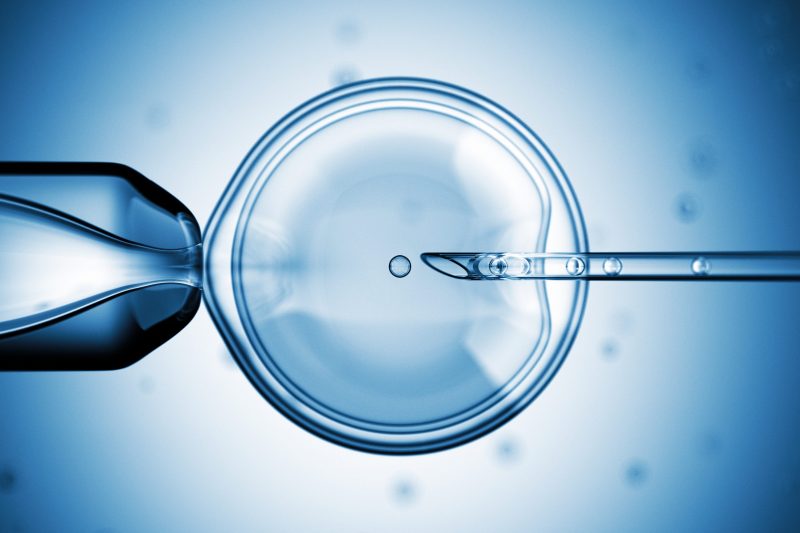
اساس آزمایش PGD
آزمایش PGD چیست؟ تشخیص ژنتیکی پیش از لانه گزینی (PGD) یکی از روش هایی است که برای پیشگیری از یک بارداری با یک بیماری ژنتیکی یا کروموزومی، در IVF کاربرد دارد. در روش تشخیص ژنتیکی پیش از لانه گزینی (PGD) سلول یا سلول هایی را از جنین در روز سوم یا پنجم تکوین جنینی جدا نموده و از نظر ژنتیکی آنها را مورد بررسی قرار می دهند. سپس جنین هایی که نرمال هستند به رحم مادر منتقل می گردند.
با انجام تست تشخیص ژنتیکی جنین پیش از لانه گزینی (PGD) می توان بیش از 100 مشکل ژنتیکی را بررسی کرد و از انتقال آنها به فرزندان بعدی جلوگیری کرد و همینطور با انجام تست تشخیص ژنتیکی جنین پیش از لانه گزینی (PGD)، باز هم نیاز به انجام آزمایش ها و غربالگری های دوران بارداری وجود دارد.
به دلیل سن بالای مادر، وجود سابقه خانوادگی بیماری های ژنتیکی، بیماری های ژنتیکی در بین زوجین و عواملی از این قبیل می تواند باعث افزایش خطر بروز ناهنجاری های کروموزومی در نوزاد شود. پیش از این روش های تشخیصی ژنتیکی پیش از تولد (PND) به منظور بررسی ناهنجاری های کروموزومی استفاده می شد، اما دربین بسیاری از زوج ها پذیرفتن آزمایش پیش از تولد به دلیل تشخیص ناهنجاری در جنین که با احتمال خاتمه حاملگی همراه است بسیار مشکل بوده و صدمات جسمی و روانی را در پی دارد. بنابراین در مورد برخی از این زوج ها تشخیص ژنتیکی پیش از لانه گزینی (PGD/preimplantation Genetic Diagnosis) به عنوان یک گزینه قابل پذیرش است.
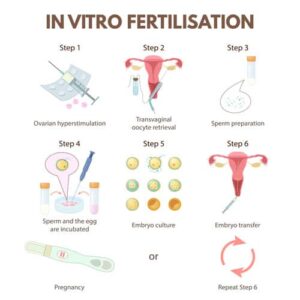
دومین گروه بزرگ انتخاب کنندﮤ PGD، کسانی هستند که مبتلا به باروری ضعیف (Sub fertility) یا ناباروری هستند و امیدوارند که با ترکیبی از تکنولوژی های تولید مثلی کمک شده و تست های ژنتیکی بر روی رویان اولیه، صاحب فرزند شوند. اساس این روش به این صورت است که به زنان به منظور تحریک تخمک گذاری زیاد (hyper ovulation) هورمون داده می شود و این تخمک ها تحت هدایت اولتراسونوگرافی و در شرایط مصرف داروی مسکن اووسیت ها از طریق دهانه رحم جمع آوری می شوند.
اسپرم های متحرک گرفته شده از یک نمونه مایع منی دریک محیط کشت به اووسیت ها اضافه می شوند(به این روش لقاح در شیشه (in vitro fertilization/IVF) گفته می شود و همان روشی است که برای درمان ناباروری استفاده می شود) و تحت شرایط انکوباسیون به اووسیت ها اجازه باروری داده می شود و یا لقاح با استفاده از تزریق درون سیتوپلاسمی اسپرم ( ICSI/intracytoplasmic sperm injection)انجام می شود. در مرحله بعد باید از یک بلاستومری که از یک بلاستوسیت جدا شده آنالیز ژنتیکی انجام شود.
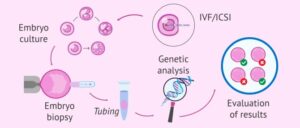
در مرحله هشت سلولی در روز سوم، یک یا گاهی دو سلول (بلاستومر) برای آنالیز از جنین اولیه، بیوپسی می کنند. توجه کنید که صرف نظر از نوع آنالیز ژنتیکی که قرار است انجام شود، امکان انجام آن بر روی مواد ژنومی برگرفته از یک سلول منفرد ضروری است و در بسیاری از موارد روش انتخابی، آنالیز با یک روش تکثیر ژنومی به نام واکنش تکثیر با جایگزینی های متعدد و مارکرهای هاپلوتایپ که به این روش تهیه هاپلوتایپ ژنتیکی پیش از لانه گزینی( haplotyping preimplantation genetic) هم می گویند است که از سال 2006 به کار می رود.
آزمایش PGD منشاﺀ والدی آلل توارثی را مشخص می کند و احتمال آلودگی با نمونه DNA خارجی را مثل مشکل حذف آللی (allele dropout) یا همان عدم تکثیر آللی که نقص در تکنیک است کاهش می دهد، در نتیجه کارایی و بازدهی روش به طور قابل توجهی افزایش پیدا می کند. حالا بعد از بیوپسی از بین رویان های بررسی شده، دو رویان سالم و غیرمبتلا را دوباره به درون رحم مادر انتقال می دهند. در یک حاملگی موفق لانه گزینی باید رخ دهد و این یک مانع بزرگ است به این دلیل که درصد موفقیت در هر بار آزمایش حتی در بهترین مراکز 30% است.
یک روش مشابه دیگر، برداشت اولین و اغلب دومین گویچه قطبی از اووسیت لقاح نیافته، در زیر زونا پلوسیدا (zona pellucida) است. آنالیز بسیار سریع، 6 ساعت بعد از برداشتن اولین گویچهٴ قطبی به دلیل تخریب سریع آن ضروری است. آنالیز گویچه های قطبی یک روش غیر مستقیم تعیین ژنوتیپ است، به این دلیل که جسم قطبی اولیه و اووسیت هر دو در حین تقسیم میوز I از هم تفکیک شده و بنابراین حاوی اعضای مختلفی از هر جفت کروموزوم های همولوگ است.
از نظر آماری تاثیر آزمایش PGD تا به حال اندک بوده، ولی طیف وسیع در حال از بیماری های ژنتیکی تا به امروز با این روش مورد آزمایش قرار گرفتند که هر کدام از آنها نیاز به یک مجوز دارند. رایج ترین موارد استفاده ازاین روش برای بیماری های تک ژنی، فیبروز کیستیک، دیستروفی میوتونیک، بیماری هانتینگتون، بتا تالاسمی، آتروفی عضلانی – نخاعی و سندروم X شکننده است.
روش شناسایی آلل های طبیعی و غیر طبیعی در این روش در صورت مناسب بودن آنالیز پیوستگی DNA، روش PCR است. انتخاب جنسیت در مورد بیماری های وابسته به X جدی در شرایطی که انالیز تک ژنی امکان پذیر نیست، انجام می گیرد.
اما بزرگترین گروه ارجاع داده شده به PGD، ناهنجاری کروموزومی و به طور خاص جابه جایی های دوطرفه و روبرت سونین است. در سال های اخیر، PGD در مواردی خاص هم برای انتخاب جنین های غیر مبتلایی که در معرض بیماری های ژنتیکی هستند، به کار می رود، هم برای ایجاد یک فرد سازگار از لحاظ آنتی ژنی لکوسیت انسانی (HLA) استفاده می شود به طوری که فرزند جدید می تواند به عنوان دهنده مغز استخوان به خواهر یا برادر مبتلای بزرگتر خود، به عنوان مثال برای کم خونی فانکونی مورد استفاده قرار می گیرد.
مزایا و معایب تکنیک تشخیص ژنتیکی جنین پیش از لانه گزینی (PGD)
مزایای آزمایش PGD
- با این روش می توان بیش از 100 مشکل ژنتیکی را بررسی کرد و از انتقال آنها به فرزندان بعدی جلوگیری کرد.
- انجام این روش همانطور که از نامش پیداست، پیش از لانه گزینی (PGD) انجام می شود، بنابراین جنین های سالم تر به رحم مادر منتقل خواهند شد در نتیجه شانس موفقیت آمیز بودن و تولد نوزاد سالم بیشتر خواهد شد.
معایب آزمایش PGD
- تعداد زیادی از متخصصان ژنتیک باوردارند که به دلیل اینکه زندگی از نطفه آغاز می شود، از بین بردن جنین های ناسالم اخلاقی نیست.
- در حالیکه PGD به کاهش احتمال ابتلای جنین به اختلالات ژنتیکی کمک زیادی می کند، ولی نمی تواند این خطر را کاملا از بین ببرد. در برخی موارد، آزمایشات بیشتری در طول بارداری مورد نیاز است تا مطمئن شویم که آیا بیماری ژنتیکی وجود دارد یا خیر.
- برخی از بیماری ها تنها زمانی که والدین به سن بالا برسند، بوجود می آیند،بنابراین هنوز این اختلالات موضوع بحث ارائه دهندگان خدمات بهداشتی است.
- توجه داشته باشید که با انجام تست تشخیص ژنتیکی جنین پیش از لانه گزینی (PGD)، باز هم نیاز به انجام آزمایش ها و غربالگری های دوران بارداری وجود دارد.
تشخیص ژنتیکی جنین پیش از لانه گزینی (PGD)در آزمایشگاه که در کلینیک های ژنتیک و IVF وجود دارد، انجام می شود. بهتر است آزمایش PGD را در مراکز درمان ناباروری که مجهز به آزمایشگاه ژنتیک نیز هستند، انجام دهید، تا مشکل حمل و نقل جنین از محلی به محل دیگر وجود نداشته باشد و شانس موفقیت افزایش یابد.
برخی از بیماری هایی که در مورد آنها تشخیص ژنتیکی پیش از لانه گزینی انجام شده و یا در دسترس است را معرفی می کنیم:
- بیماری هایی با توارث اتوزوم غالب: شارکوت ماری- توث، آدنوماتوز پولیپوز خانوادگی، بیماری هانتینگتون، سندرم مارفان،دیستروفی میوتونیک، نوروفیبروماتوز، استئوژنزایمپرفکتا، توبروز اسکلروزیس
- بیماری هایی با توارث آتوزوم مغلوب: بتا تالاسمی، فیبروز کیستی، اپیدرمولایزز بلوزا، بیماری گوشه، بیماری کم خونی داسی شکل، آتروفی عضلانی – نخاعی، بیماری تای – ساکس
- بیماری هایی با توارث وابسته به X: سندرم آلپورت، دیستروفی عضلانی دوشن (DMD)، سندرم هانتر، سندرم کندی (kennedy)، سندرمX شکننده
- بیماری هایی با توارث وابسته به X که در این مورد فقط تعیین جنسیت انجام می شود: نقص اورنیتین ترانس کربامیلاز،DMD، اینکانتنی ننتا پیگمنتی
- بیماریی های با توارث میتوکندریایی: (MELAS) میوپاتی میتوکندریایی انسفالوپاتی اسیدوز لاکتیک و حملات شبه سکته ای
- بیماری هایی با توارث کروموزومی: جابه جایی روبرتسونی، جابه جایی دوطرفه، غربالگری آنیوپلوئیدی، وارونگی ها، حذف شدگی ها
MELAS (: Mمیوپاتی میتوکندریایی، E: انسفالوپاتی، LA: اسیدوز لاکتیک، S: حملات سکته)