آزمایش CVS تست تهاجمی برای تشخیص نقص های مادرزادی و اختلالات کروموزومی پیش از تولد
آزمایش CVS یا نمونه برداری از پرزهای جفتی به این صورت است که تکه کوچکی از پرزهای سطح خارجی جفت برداشته شده و کاریوتایپ جنین را تهیه می کنند و یا برای بررسی مولکولی بیماری های ژنتیکی به آزمایشگاه ژنتیک فرستاده می شود. این بافت منشا جنینی دارد، که از لایه سلولی خارجی بلاستوسیت (تروفوبلاست) مشتق شده است.
نمونه پرزهای کوریونی (CVS) تقسیم شده و یک بخش آن برای تهیه کشت سلول مورد استفاده قرار می گیرد. از بخش دیگر DNA استخراج می شود تا بیماری های ژنتیکی ای که جنین در معرض ابتلا به آنهاست مورد بررسی قرار می گیرند، به عبارتی آزمایش مستقیم جهش یا گاهی بررسی مجموعه مارکرهای هاپلوتایپ پر خطر (high risk set of haplotype markers) انجام می شود.
برای آنیوپلوئیدی های شایع، آزمایش QF-PCR معمولا بکار می رود که در ادامه آنالیز کامل کاریوتایپ و گزارش آن بعد از کشت سلول انجام می شود. آزمایش ها گاهی به صورت بیوشیمیایی (به عنوان مثال نقایص مادر زادی متابولیسمی) هستند. این آزمایش ها بر روی نمونه بافت قابل انجام است و اگر نمونه خیلی کوچک باشد، بعد از کشت سلول، آزمایش انجام می شود.
خطر آزمایش CVS
خطر سقط جنین در این روش معمولا 1% است، هر چند اگر نمونه برداری توسط افراد ماهر و با تجربه انجام شود میزان خطر کمتراست.
روش کار/ پروتکل جمع آوری و انتقال نمونه
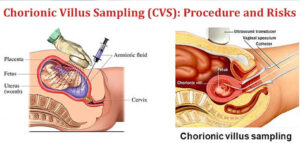
نمونه CVS از طریق شکم یا از طریق سرویکس، همانطور که در بالا اشاره شد، بین هفته 12-10 حاملگی گرفته می شود. پرزهای جفتی با مقدار کمی محیط ترنسپورت که شامل هپارین است آسپیره می شود و داخل catheter نمونه گیری (هپارین) برای جلوگیری از لخته شدن خون اطراف villi به کار می رود.
تو شرایط استریل، پرزها به یک فلاسک یا لوله که شامل محیط ترنسپورت است منتقل می شود. نمونه باید به آزمایشگاه با سرعت هر چه ممکن منتقل شود، گرچه محیط ترنسپورت نمونه را برای ۳-۲ روز نگه می دارد، ولی نکته مهم این است که هر تاخیر در انتقال، شانس موفقیت با کشت کوتاه مدت را کاهش می دهد.
شرایط و اندازه نمونه CVS
شرایط و اندازه هر نمونه خیلی متفاوت است و به محل جفت، روش نمونه برداری و کسی که نمونه را می گیرد، بستکی دارد. معمولا mg20 نمونه پرز جفتی برای شروع هر دو کشت بلند مدت و کوتاه کافی است.
بهترین ناحیه جفت برای نمونه برداری از پرزهای جفتی، فروندوسوم جفت است چون این ناحیه بهترین کیفیت پرزها را دارد. نواحی دیگه برای نمونه برداری، خصوصا در دومین و سومین سه ماهه اول حاملگی احتمال بیشتری دارد که با جفت مادری و نواحی degenerative ویلی آلوده باشد. بیشتر نمونه ها با اجزاء خون مادر یا بافت جفت، یا هر دو، آلوده اند، که برداشتن آن ها قبل از کشت، ضروری است.
تست های اضافی
به این دلیل که CVS شمار زیادی، سلول فعال، از نظر متابولیسم فراهم می کند. این موضوع ارزیابی مستقیم اختلالات ارثی متابولیکی و ممکن می کند. معمولا مواد کافی برای استخراج DNA از ویلی های تمیز شده برای اختلالات تک ژنی جهت تحقیق و بررسی وجود دارد. بررسی CVS سه ماهه اول، یک روش تشخیص انتخابی، برای خانواده هایی با تاریخچه بیماری های بیوشیمیایی یا اختلالات مولکولی است.
پرزهای کوریونی چیست؟ محتویات سلولی
CVS از سه لایه تشکیل شده:
۱-سینسیتیوتروفوبلاست (syncytiotrophoblast) خارجی
۲-سیتوتروفوبلاست (cytotrophobast)داخلی
3- هسته مزانشیمی داخلی
این انواع سلولی منشاء های متفاوتی دارند که آزمایش دو رده سلولی را ممکن می سازد. لایه سیتوتروفوبلاست شامل سلول هایی است که خود به خود تقسیم می شود و می تواند در متافاز متوقف شوند و بعد از کشت کوتاه مدت آزمایش می شوند، بنابراین سلول های مزانشیال هسته Villus در کشت بلند مدت رشد داده می شود.

ماندگاری کشت، هاروست و تهیه کروموزوم
کشت coverslip که آماده شد، دو یا سه قطره فیکساتیو را برای برداشتن لامل از ظرف اضافه کرده و گستره های مناسب از کروموزوم های CVS تهیه کنید. کشت های لوله یا فلاسک ها می بایست بعد از ۳-۲ روز بررسی شوند، و وقتی رشد را مشاهده کردید، محیط عوض شود. معمولا پس از بیشتر از ۲ روز، محیط دوباره عوض می شود، و یا روزانه تعویض شده تا برای هاروست آماده شود. هاروست و تهیه اسلاید قبلا برای مایع آمنیوتیک شرح داده شده است.
روش کار/پروتکل کشت بافت های جامد مثل C.V.S و P.O.C
۱-برای آماده سازی نمونه جهت کشت، در صورتیکه نمونه C.V.S باشد بصورت زیر عمل کنید:
الف) نمونه مورد نظر را شستشو داده تا از خون و موکوس عاری شود.
ب) سپس با سر سوزن بافت های مادری، از قبیل خون را جدا کنید.
ج) سپس با اسکالپل استریل، نمونه را به قطعات بسیار ریز تقسیم کرده، و از نمونه حاصل، سوسپانسیون سلولی تهیه کنید، و با توجه به مقدار نمونه، و نوع ظرف به آن، محیط اضافه کنید.
۲- تمامی مراحل دیگر کاملا مشابه کشت AF است.
برای کشت نمونه های P.O.C با توجه به اینکه کدام بافت را برای کشت برداشتیم C.V.S، پوست یا بند ناف یا کیسه آمنیوتیک به صورت زیر انجام دهید:
الف) نمونه مورد نظر را شستشو داده (با محیط) تا از خون و موکوس عاری شود.
ب) سپس با اسکالپل استریل آن را به قطعات بسیار ریز تقسیم کرده و سوسپانسیون سلولی را کشت دهید.
۴- بعد از ۷-۵ روز نمونه را به آرامی از انکوباتور خارج و با invert microscope آن را بررسی کنید. در صورت مشاهده کلونی، محیط آن را برداشته و با محیط تازه تعویض کنید.
۵- دو روز در میان ،نمونه ها را با invert microscope بررسی کرده و محیطش را عوض کنید.
6- بعد از رشد کلونی به اندازه کافی می توانیم یکی از لوله ها را هاروست کنیم و لوله دیگر را subculture دهیم.
۷- subculture دادن نمونه، به این صورت است که نمونه مورد نظر را انتخاب کرده، سپس محیط آن را در لوله ای جداگانه می ریزیم. سپس نمونه را با PBS با دمای 37 درجه سانتیگراد شستشو داده و محلول آن را به لوله فوق اضافه می کنیم.
۸- الف- در لوله Lighton 0.5cc و به فلاسک 1 cc محلول trypsin-EDTA(1X) با دمای 37، درجه سانتیگراد بریزید و آن را به مدت ۳۰ ثانیه درون ۳۷ درجه سانتیگراد قرار دهید.
ب- با جدا شدن سلول از سطح ظرف کشت، برای خنثی کردن اثر trypsin به آن 1cc محیط کامل حاوی سرم اضافه کنید.
ج- سپس با توجه به مقدار نمونه درون ظرف های دیگر آن را aliquot می کنیم و در انکوباتور ۳۷ درجه سانتیگراد قرار می دهیم. ( قسمت ۳و۷ فقط برای subculture دادن نمونه ها است).
۹- برای هاروست، به ازای هر 1cc حدودا ۷۵ میکرولیتر کلسمید اضافه کرده، و ۴-۳ ساعت در ۳۷ درجه انکوبه کنید. پس از این مدت طبق قسمت شماره ۷ سلول ها را trypsinized کنید و سوسپانسیون سلولی رو در لوله جداگانه نگهداری کنید.
۱۰- بعد از جدا شدن و جمع آوری سوسپانسیون، آن را به مدت ۱۵ دقیقه با دور 1000rpm سانتریفوژ کنید.
۱۱- supernatant را برداشته و به آن محلول هایپوتونیک 0.06 M از KCL اضافه کنید و به مدت ۱۰ دقیقه در ۳۷ درجه سانتیگراد انکوبه کنید.
۱۲- سپس سانتریفوژ کرده، و بعد از حذف supernatant به آن Fix 3:1 5cc (متانول: اسیداستیک) اضافه کرده و ۲۰ دقیقه آن را به همین حالت قرار دهید.
۱۳- بعد از ۲۰ دقیقه، نمونه را سانتریفوژ کرده و مجددا fix اضافه کنید و20 دقیقه دیگر در همین حالت قرار دهید.
۱۴- سپس نمونه را سانتریفوژ، و غلظت سوسپانسیون را جهت لام گیری آماده کرده، و از نمونه لام گیری کنید.
مراحل 8-1 در شرایط استریل انجام می شود.
هفت روز بعد از کشت، نمونه ها را از انکوباتور خارج کنید و با میکروسکوپ اینورت مشاهده کنید و در صورت مشاهده کلونی ( سلول های دوکی شکل) محیط را با محیط تازه عوض کنید. پس از دو روز نمونه ها از انکوباتور خارج و در زیر میکروسکوپ اینورت مشاهده کنید، و اگر دیدید که نمونه ها رشد کافی دارند، آن ها را برای ساب کالچر و هاروست مستقیم بردارید.
روش کار/نحوه انجام ساب کالچر در آزمایش CVS
محیط رویی لیتون را در یک فالکون ۵۰ خالی کنید. با PBS 0.5cc شستشو و در فالکون خالی کنید. دوباره PBS 0.5cc و در فالکون خالی کنید. حال 0.5 cc تریپسین EDTA را در لیتون ریخته و بگذارید به مدت ۳۰ ثانیه، در دمای ۳۷ درجه بماند. بعد از اون لیتون را خارج کرده، و ضربه به لبه انکوباتور بزنید، و سپس در زیر میکروسکوپ اینورت مشاهده کنید.
در صورتی که سلول ها گرد شده بودن، یعنی اینکه کار شما درست و سلول ها تریپسینایز شدند. و اگر بلند نشده بودند، باید کمی صبر کنید. بعد بر روی آن 3 cc محیط تازه آمنیومکس بریزید (جهت توقف عمل تریپسین)، و به دو لوله لیتون تقسیم کنید و در انکوباتور ۳۷ درجه سانتیگراد بگذارید و ۴۸-۱۲ ساعت هاروست کنید. بهتر است که لوله ها را ۱۲ ساعته هاروست کنید، یعنی ۸ شب ساب کالچر، و ۸ صبح هاروست کنید. اگر چند ساعت بعد از ساب کالچر، نمونه ها را مجددا با میکروسکوپ اینورت ببینید، متوجه می شوید که سلول ها چسبیده اند.
روش کار/نحوه انجام هاروست در آزمایش CVS
به یکی از لوله های کم سلول تر، 0.5 cc کلسمید افزوده و لوله را در انکوباتور ۳۷ درجه سانتی گراد، به مدت ۴-۳ ساعت بگذارید. سپس هاروست را شروع کنید. ابتدا محلول رویی(سوپرناتانت) را در یک فالکون بریزید. و بار دوم با PBS 0.5 cc شستشو داده و در فالکون بریزید. بار آخر 0.5 cc تریپسین EDTA بر روی سلول ها ریخته و بگذارید ۳۰ ثانیه یا 0.5 دقیقه در ۳۷ درجه سانتیگراد بماند.
پس از آن لوله را خارج کرده و محتویات فالکون روبر روی آن بریزید و هاروست را شروع کنید. ابتدا بگذارید به مدت ۱۰ دقیقه با دور 1300 ساتریفوژ شود. و بعد از آن محلول روئی را خالی کرده و برروی آن 8 cc محلول هایپوتونیک بریزید، و به آرامی بهم بزنید، و بگذارید ۵ دقیقه در بن ماری ۳۷ درجه و یا انکوباتور ۳۷ درجه بماند.
سپس سه قطره فیکس بر روی آن ریخته و بگذارید به مدت ده دقیقه با دور۱۰۰۰ سانتریفوژ شود. بعد لوله را خارج کرده محلول رویی را بیرون ریخته و بر روی آن ابتدا 3ccفیکس 3:1 قطره قطره اضافه کنید، و سپس 5-9cc فیکس بعدی رو بر روی آن اضافه کنید.
سپس لوله را به مدت ۱۰ دقیقه با دور ۱۳۰۰ سانتریفوژ کنید، و سپس لوله را خارج کرده محلول رویی را بیرون بریزید، و بر روی آن مجددا 12cc فیکس آرام آرام اضافه کنید. سپس لوله را به مدت ۱۰ دقیقه با دور ۱۳۰۰ سانتریفوژ کرده و سپس لوله رو خارج کرده و محلول رویی را بیرون ریخته (در همه مراحل از پیپت پاستور برای کشیدن محلول رویی و دور ریختن آن استفاده کنید).
سپس بر روی آن چند قطره فیکس ریخته و لام گیری کنید. لام گیری از فاصله نزدیک، بر روی لام های تمیز شده با اتانول، انجام می شود، یعنی در واقع لام گیری touch است. برای ایجاد شرایط بهتر لام گیری، از یک چراغ مطالعه و دستمال کاغذی خیس که لام ها را برروی آن می گذارید، و چراغ مطالعه که بخار ایجاد می کند، می شود استفاده کرد.
کشت CVS زیر هود لامینار
نمونه مورد نظر را در یک پتری دیش استریل ریخته و سپس برروی آن PBS بریزید تا کاملا خون آن شسته شود، همچنین پرزها را رگ های خونی را جدا کنید. چندین بار این شستشو را ادامه دهید و با پیپت پاستور در زیر هود، محیط پس مانده را عوض کنید.
در پایان وقتی کاملا پرزها و رگ های خونی جدا شد و PBS سفید و بافت نیز سفید بود، کار را شروع کنید قبل از شروع 1 cc کلاژناز و 0.5cc تریپسین EDTA اضافه کرده، با اسکالپل و پنس نمونه را با پنس گرفته و با اسکالپل ضربات متوالی و سریع به بافت بزنید، تا کاملا خرد شود بعد از اینکه به قطعات ریز تقسیم شد، از سوسپانسون حاصل، در چهار لوله لیتون کشت دهید، و روی هر کدوم 1.5 cc محیط آمنیومکس اضافه کنید. بعد در انکوباتور ۳۷ درجه بگذارید بماند. بعد از ۷-۵ روز نمونه ها را از انکوباتورخارج کرده، و در زیر میکروسکوپ اینورت بررسی کنید.
در صورت رشد کلونی های سلولی و حالت خوشه ای، رشد سلول های دوکی، نمونه را یا هاروست واگر رشد کافی نداشت تعویض محیط کنید.
تذکر: پروتکل ها آزمایش CVS بر اساس setup آزمایشگاه ها متفاوت است.
بیشتر بدانید:










































