حامل های کلونینگ یوکاریوت ها و کلونینگ فراتر از مطالعه یک ژن(پلاسمید های الحاقی و پلاسمیدهای تکثیر شونده مخمر)
بیشتر آزمایشات کلونینگ با استفاده از E.coli به عنوان میزبان انجام شده است و متنوع ترین وکتورهای کلونینگ برای این میزبان در دسترس است. زمانی که هدف از آزمایش کلونینگ بررسی ویژگی های پایه ای بیولوژی مولکولی مثل ساختار و عملکرد ژن باشد، E.coli به طور ویژه مدنظر می باشد.
به هرحال تحت بعضی شرایط، ممکن است در آزمایشات کلونینگ نیاز به استفاده از میزبان یوکاریوتی داشته باشیم. این مورد خصوصا در بیوتکنولوژی، جایی که هدف از کلونینگ مطالعه یک ژن نیست بلکه به دست آوردن مقدار زیادی از یک پروتئین دارویی مهم یا تغییر خصوصیات یک ارگانیسم می باشد، بیشتر صحت پیدا می کند. بنابراین بایستی به وکتورهای کلونینگ برای میزبان هایی غیر از E.coli نیز فکر کنیم.
وکتور هایی برای مخمر و دیگر قارچ ها
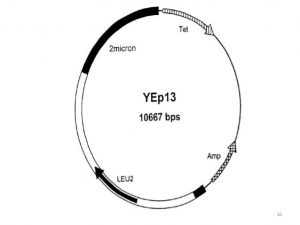
یکی از مهم ترین ارگانیسم ها در بیوتکنولوژی، مخمر ساکارومایسس سرویزیه است. مخمر علاوه بر نقشی که در تخمیر و تهیه نان دارد، به عنوان یه ارگانیسم میزبان برای تولید مواد دارویی مهمی از ژن ها ی کلون شده نیز مورد استفاده قرار می گیرد. ساخت وکتورهای مخصوص مخمر در ابتدا با کشف پلاسمیدی که در بیشتر سویه های ساکارومایسس سرویزیه وجود داشت آغاز شد. این پلاسمید یکی از معدود پلاسمید هایی است که در سلول های یوکاریوتی یافت شده است، پلاسمید μm2 نامیده می شود.
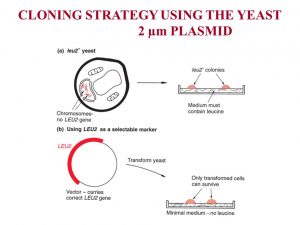
مارکر های قابل انتخاب برای پلاسمید 2μm
برای ساخت وکتورهای کلونینگ، استفاده از پلاسمید 2 μm بسیار مناسب می باشد. اندازه ی آن 6 kb است که برای یک وکتور مناسب است و تعدادکپی های آن بین 70 تا 200 عدد در سلول مخمر است. تکثیر با استفاده از مبدا همانندسازی پلاسمید صورت می گیرد و تعدادی از آنزیم های مورد نیاز توسط سلول میزبان فراهم می شود و پروتئین ها نیز توسط ژن های REP1 و REP2 که توسط پلاسمید حمل می شوند کد می گردند.
اما با وجود همه این موارد، باز هم استفاده از پلاسمید 2 μm به عنوان وکتور کلونینگ خیلی ساده نیست. بیشتر وکتورهای مخمری از نوعی سیستم انتخاب گر کاملا متفاوت برخوردار هستند در عمل جهت داشتن مارکر انتخاب گر، از ژن طبیعی مخمر که به طور معمول آنزیم مورد نیاز برای بیوسنتز یک آمینواسید را کد می کند استفاده می شود.
یک نمونه از این ژن ها، LEU2 می باشد که آنزیم بتا ایزوپروپیل مالئات دهیدروژناز را کد می کند. این آنزیم در تبدیل پیرویک اسید به لوسین نقش دارد. وکتورهایی که از پلاسمید 2μm مشتق شده اند، پلاسمیدهای اپی زومال مخمر (YEPS) نامیده می شوند. تعدادی از YEPها دارای کل پلاسمید 2μm هستند و بعضی تنها حاوی مبدا همانندسازی این پلاسمید می باشند که مثال این نوع پلاسمید YEP13 می باشد.
این وکتور شاتل (دو گانه) است و علاوه بر مبدا همانندسازی پلاسمید 2 μm و ژن انتخاب گر LEU2 دارای کل توالی PBR322 نیز می باشد. بنابراین می تواند هم در مخمر و هم در E.coli همانندسازی کند و تحت انتخاب قرار بگیرد. جهت استفاده از وکتورهای شاتل دلایل متعددی وجود دارد.
یک دلیل اینکه ممکن است بازیابی دوباره مولکول DNA نوترکیب از کلونی مخمر ترانسفورم شده مشکل باشد، چنین مشکلی در مورد YEP وجود ندارد چرا که از ابتدا در سلول مخمر به صورت پلاسمیدی وجود داشته است، اما در رابطه با دیگر وکتورهای مخمر که ممکن است به یکی از کروموزوم های مخمر الحاق یافته باشند، تخلیص پلاسمید را غیر ممکن می سازد. برای چنین وکتورهایی این یک عیب محسوب می شود چون در بسیاری از آزمایشات کلونینگ، تخلیص DNA نوترکیب به منظور تعیین ساختار صحیح آن، برای مثال توالی یابی DNA ضروری است.
علاوه بر YEP ها، چندین نوع دیگر از وکتورهای کلونینگ جهت استفاده در ساکارومایسس سرویزیه وجود دارند، که به 2 تا از مهم ترین آن ها اشاره می کنیم:
1- پلاسمید های الحاقی مخمر(YIpS): اساسا پلاسمید های باکتریایی هستند که حامل یک ژن مخمری می باشند. به عنوان مثال می توان Yips را نام برد که یک پلاسمید PBR322 در بردارنده ی یک ژن URA3 می باشد. این ژن آنزیم اوروتیدین5-فسفات دکربوسیثلاز را کد می کند. (آنزیمی که یکی از مراحل بیوسنتز نوکلئوتیدهای پریمیدینی را کاتالیز می کند) و به عنوان مارکر انتخاب گر دقیقا به روش مشابهی با LEU2 مورد استفاده قرار می گیرد. Yip مانند یک پلاسمید قادر به همانندسازی نیست، چون دارای هیچ قسمتی از پلاسمید 2μm نمی باشد به طوری که برای بقای خودش وابسته به الحاقش به داخل DNA کروموزومی مخمر است.
2- پلاسمیدهای تکثیر شونده مخمر(YRpS): قادرند همانند پلاسمید های مستقل تکثیر شوند، به این دلیل که آن ها توالی DNA کروموزومی که حاوی مبدا همانندسازی می باشد را حمل می کنند. مشخص شده است که مبداهای همانندسازی در نزدیکی چندین ژن مخمر قرار گرفتند که از جمله آن ها می توان به یک یا دو ژن اشاره کردکه می توانند به عنوان مارکرهای انتخابگر مورد استفاده قرار گیرند. وکتور YRp7 یک نمونه از پلاسمیدهای تکثیر شونده است. این وکتور از پلاسمید PBE322 به علاوه ژن TRP1 مخمر ساخته شده است. این ژن که در بیوسنتز تریپتوفان نقش دارد در نزدیکی مبداهمانندسازی واقع شده است . قطعه DNA مخمر که در YRp7 وجود دارد حاوی هم ژن TRP1 و هم مبدا هماندسازی است.
انواع دیگر وکتورهای کلونینگ مخمر و استفاده از کروموزوم های مصنوعی برای کلون کردن قطعات بزرگ DNA در مخمر
علاوه بر yep ها چندیدن نوع دیگر از وکتور های کلونینگ جهت استفاده در ساکاروماسیس سرویزیه وجود دارند .
پلاسمید های الحاقی مخمر :(yips) اساسا پلاسمید های باکتریایی هستند که حامل یک ژن مخمری می باشند. به عنوان مثال می توانYIps را نام برد که یه پلاسمید Pbr322 دربردارنده یک ژن URA3 می باشد. این ژن آنزیم اوروتیدین ۵-فسفات دکربوکسیلاز را کد می کند (آنزیمی که یکی از مراحل بیوسنتز نوکلئوتید های پیریمیدینی را کاتالیز می کند) و به عنوان مارکر انتخابگر دقیقا به روش مشابهی با LEU2 مورد استفاده قرار می گیرد.
Yip مانند یک پلاسمید قادر به همانندسازی نیست، چون دارای هیچ قسمتی از پلاسمید 2 um نمی باشد به طوری که برای بقای خودش وابسته به الحاقش به داخل DNA کروموزومی مخمر است. الحاق به کروموزوم درست مثل آنچه در مورد Yep توضیح داده شد، انجام می شود .
پلاسمید های تکثیرشونده مخمر (YRpS) قادرند همانند پلاسمید های مستقل تکثیر شوند، به این دلیل که آن ها توالی DNA کروموزومی که حاوی مبدا همانندسازی می باشد را حمل می کنند. مشخص شده است که مبداهای همانندسازی در نزدیکی چندین ژن مخمر قرار گرفته اند که از جمله آن ها می توان به یک یا دو ژن اشاره کرد که می توانند به عنوان مارکر های انتخابگر مورد استفاده قرار گیرند.
وکتور YRP7 یک نمونه از پلاسمید های تکثیرشونده است. این وکتور از پلاسمید PBR322 به علاوه ژن TRp1 مخمر ساخته شده است. این ژن که در بیوسنتز تریپتوفان نقش دارد در نزدیکی مبدا همانندسازی واقع شده است. قطعه DNA مخمر که YRPوجود دارد حاوی هم ژن TRP و هم مبدا همانندسازی است .
سه عامل در تصمیم گیری جهت انتخاب وکتور مناسب برای کلونینگ ژن ها در مخمر نقش بازی می کنند. اولین عامل فراوانی ترانفورماسیون است که مقیاس آن تعداد سلول های ترانسفورم شده می باشد که می تواند به ازای هر میکروگرم از DNA پلاسمید بدست آید. اگر مقدار DNA اولیه کم باشد یا نوترکیب های زیادی لازم باشد، فراوانی ترانسفورماسیون بالایی مورد نیاز است.
YEP ها دارای بالاترین توانایی ترانسفورماسیون هستند که بین هزار تا صد هزار ترانسفورم شده را به ازای هر میکروگرم DNA فراهم می کنند. YRP ها نیز خیلی مولد و پربازده هستند به طوری که هزار تا ده هزار سلول ترانسفورم شده را به ازای هر میکروگرم DNA تولید می کنند، اما بازده YIP کمتر از هزار است و فقط 10-1 سلول ترانسفورم شده به ازای هر میکروگرم حاصل می شود، مگر اینکه روش خاصی به کار گرفته شده باشد . پایین بودن فراوانی ترانسفورماسیون YIP نشان دهنده این واقعیت است که قبل از ماندگاری وکتور در داخل مخمر ، پدیده نسبتا نادر الحاق به داخل کروموزوم لازم است .
دومین عامل مهم تعداد کپی می باشد . YEP ها و YRP ها بیشترین تعداد کپی را دارا هستند که به ترتیب دارای 50-20 و 100-5 کپی می باشند . بر خلاف آن ها از YIP تقریبا یک کپی در هر سلول حضور دارد. این دو عامل ، چنانچه هدف به دست آوردن پروتئین از ژن های کلون شده باشد مهم هستند، چرا که هر چه تعداد کپی ها از ژن مورد نظر بیشتر باشد میزان بازده فراوانی پروتئینی قابل انتظار نیز بیشتر خواهد بود .
چرا تمایل به استفاده از YIP ها وجود دارد؟ جواب این است که این وکتور ها ، نوترکیب های بسیار پایداری ایجاد می کنند به طوری که از دست رفتن YIP هایی که به داخل کروموزوم وارد شده اند به مقدار خیلی کمی اتفاق می افتد. برعکس، نوترکیب های YRP بسیار ناپایدار هستند، به طوری که در هنگام جوانه سازی سلول های دختری، پلاسمید ها تمایل به تجمع در سلول مادری دارند که این باعث غیرنوترکیب شدن سلول دختری می شود.
نوترکیب های YEP از مشکلات مشابهی رنج می برند، اگر چه فهم ما از بیولوژی پلاسمید 2 UM در سال های اخیر باعث ایجاد YEP های پایدارتری شده است. با این وجود، چنانچه هدف از آزمایشات ایجاد سلول های مخمر نوترکیبی باشد که بایستی ژن کلون شده را برای مدت طولانی در خود نگه دارد ، YIP وکتور انتخابی است .
کروموزوم های مصنوعی می توانند برای کلون کردن قطعات بزرگ DNA در مخمر استفاده شوند
آخرین نوع وکتور های کلونینگ در مخمر که مدنظر قرار میگیرند، کروموزوم مصنوعی مخمر YAC است که رویکردی کاملا متفاوت را در کلونینگ نشان می دهد. ساخت YAC ها نتیجه جانبی تحقیقات بنیادی بود که روی ساختمان کروموزومی انجام شد، کاری که منجر به شناخت اجزای کلیدی کروموزوم شد.
- سانترومر که در طول تقسیم سلول برای توزیع صحیح کروموزوم ها به سلول های دختری، مورد نیاز است .
- دو تلومر، ساختار هایی در انتهای کروموزوم که برای همانندسازی صحیح انتهاها و جلوگیری از خورده شدن توسط اگزونوکلئازها ضروری هستند.
- مبدا همانند سازی ، محل هایی در طول کروموزوم هستند که همانندسازی DNA از آن ها شروع می شود و مشابه مبدا همانندسازی پلاسمید هستند .
وقتی که ساختمان کروموزوم با این روش شناخته شد، این امکان حاصل شد که بتوان با روش های نوترکیبی DNA ،اجزای مجزای کروموزوم را جدا کرده و سپس با اتصال مجدد آن ها در لوله آزمایش یک کروموزوم مصنوعی ساخت. از آنجا که مولکول های DNA موجود در کروموزوم طبیعی مخمر طولی معادل چند صد کیلوباز دارند، این امکان حاصل شد که بتوان قطعات بلندی از DNA را در کروموزوم مصنوعی مخمر کلون کرد .
ساختار و نحوه استفاده از یک وکتور YAC
چندین وکتور YAC به وجود آمده اند که هر یک به روش مشابهی ساخته شده اند و یک نمونه بارز از آن ها PYAC3 است. در نگاه اول PYAC3 شباهت زیادی به یک کروموزوم مصنوعی ندارد، ولی با بررسی بیشتر، ویژگی های منحصر به فرد آن آشکار می گردد.
PYAC3 اساسا یک پلاسمید PBR322 است که چندین ژن مخمر به درون آن ملحق شده است. دوتا از این ژن ها یعنی URA و TIP به ترتیب عنوان مارکر انتخابگر YRP و YIP معرفی شده اند. همانند YRP ، قطعه DNAای که TRP را حمل می کند مبدا همانندسازی را نیز شامل می شود، اما در PYAC3 این قطعه تا جایی گسترش می یابد که توالی CEN4، منطقه سانترومری کروموزوم 4 مخمر را در بر می گیرد. قطعه TRP1-ORIGIN-CEN4 شامل دو جز از سه جز کروموزوم مصنوعی است.
جز سوم یا تلومر ها توسط دو توالی که TEL نامیده می شوند فراهم می گردند. این دو توالی کامل نیستند ولی در هسته مخمر به عنوان توالی های مرکزی عمل می کنند که تلومر ها از روی آن ساخته خواهند شد. یک قسمت باقیمانده دیگر PUAC3 که هنوز به آن اشاره نشده است ، SUP4 است که مارکرهای انتخابگر را شامل می شود و DNA جدید در طول آزمایش کلونینگ به آن ملحق می شود.
روش کلونینگ با PYAC3
ابتدا وکتور با ترکیبی از آنزیم های محدودالاثر BamHI و SnaBI به سه قسمت بریده می شود. قطعه با دو انتهای BamHI کنار گذاشته می شود، دو بازو باقی می ماند که هر کدام دارای یک توالی TEL و یک جایگاه SnaBI است . DNAای که قرار است کلون شود باید دارای انتهاهای صاف باشد (SNABI یه برش دهنده صاف است که توالی TACGTA را مورد شناسایی قرار می دهد) که با اتصال به بین دو بازو نهایتا یک کروموزوم مصنوعی ساخته می شود.
برای ورود کروموزوم مصنوعی به داخل ساکارومایسس سرویزیه از روش ترانسفورم کردن به پروتوپلاست استفاده می شود. سویه مخمر مورد استفاده، جهش یافته دوگانه اگزوتروف URA3TRP می باشد که به وسیله دو مارکر واقع در کروموزوم مصنوعی به URA3TRP تبدیل می شود. سلول های ترانسفورم شده با کشت روی محیط حداقل کشت داده می شوند، به طوری که تنها سلول های حاوی کروموزوم مصنوعی که به طرز صحیحی ساخته شده اند قادر به رشد بوده و انتخاب می گردند.
سلول هایی که با کروموزوم مصنوعی ناصحیح ترانسفورم شده اند به جای یک بازوی چپ و یک بازوی راست از هر کدام دارای دوبازو هستند که این سلول ها قادر به رشد بر روی محیط کشت حداقل نیستند، چون که فاقد یکی از دو مارکر می باشند. به منظور بررسی وجود DNA الحاقی در وکتور می توان از روش الحاق غیرفعال کننده SUP4 استفاده کرد که با یک آزمون ساده رنگی انجام می شود، به طوری که کلون های سفید رنگ سلول های نوترکیب و کلونی های قرمز رنگ سلول های غیر نوترکیب هستند.
کاربرد وکتور های YAC :محرک اولیه جهت طراحی کروموزوم های مصنوعی مخمر، متخصصان ژنتیک بودند که می خواستند از کروموزوم های مصنوعی جهت بررسی جنبه های گوناگون ساختمان و رفتار کروموزوم، مثل بررسی جدا شدن کروموزوم ها در طی تقسیم میوز ، استفاده کنند. این آزمایشات تصدیق کردند که کروموزوم های مصنوعی در طول تکثیر پایدار هستند و این احتمال بالا رفت که کروموزوم های مصنوعی می توانند به عنوان وکتور برای ژن هایی که به خاطر طول زیادشان قادر به ورود به صورت یک قطعه منفرد به وکتور E.COLI نیستند مورد استفاده قرار بگیرند.
چندین ژن مهم در پستانداران دارای طولی بیش از 100 کیلوباز هستند(برای مثال، ژن فیبروز سیستیک انسانی 120 KB می باشد)که بیش از ظرفیت تمام وکتور های E.COLI، به جز سیستم های کلونینگ بسیار پیشرفته E.COLI است ولی به خوبی در دامنه وکتور YAC قرار می گیرند. بنابراین کروموزوم های مصنوعی مخمر راه را برای مطالعه عملکرد و نحوه بیان ژن هایی که در گذشته امکان مطالعه آن ها به روش تکنیک DNA نوترکیب وجود نداشت، باز کرد.
با کشف اینکه تحت بعضی شرایط YAC ها قادرند در سلول های پستانداران تکثیر یابند، ابعاد جدیدی از این آزمایشات فراهم گردید که ما را قادر می سازد تا بررسی عملکرد ژن را در موجودی که به طور طبیعی دارای همان ژن است انجام دهیم. کروموزوم های مصنوعی مخمر در تولید کتابخانه های ژنی هم اهمیت دارند.
به خاطر بیاورید که حداکثر طول قطعات ورودی در بزرگترین وکتور E.COLI در حدود 300KB است، که در این صورت برای ایجاد کتابخانه ژنی انسان حدود سی هزار کلون لازم است، اما وکتور های YAC معمولا برای کلون کردن قطعات 600KB مورد استفاده قرار می گیرند و انواع خاصی قادر به کلون کردن قطعات DNA تا طولی معادل 1400 کیلوباز نیز می باشند، که تعداد کلون های لازم برای تهیه کتابخانه ژنی انسان را به 6500 کلون کاهش می دهند.
متاسفانه MEGA-YAC با مشکل پایداری قطعه ورودی مواجه هستند که DNA کلون شده گاهی اوقات توسط نوترکیبی های داخل مولکولی دچار نوآرایی می شود. با این وجود YAC ها در فراهم کردن قطعات بزرگ DNA کلون شده برای استفاده در پروژه های توالی یابی DNA در مقیاس بزرگ ، ارزش زیادی دارند .
وکتورهایی برای سایر مخمر ها و قارچ ها
جهت انجام مطالعات پایه ای بیولوژی مولکولی در ارگانیسم هایی مثل مخمر و قارچ و گسترش کاربرد های احتمالی آن ها در بیوتکنولوژی، دسترسی به وکتور های کلونینگ برای دیگر گونه های مخمر ها و قارچ ها مورد نیاز است. پلاسمید های اپی زومال مبتنی بر پلاسمید 2um ساکارومایسس سرویزیه، در انواع محدودی از سایر مخمر ها قادر به همانند سازی هستند، اما دامنه این گونه ها به اندازه کافی وسیع نیست، برای اینکه وکتور های 2UM کاربرد عمومی پیدا کنند.
در هر مورد، فراهم شدن نیاز های بیوتکنولوژی به وسیله پلاسمید های الحاقی، مثل YIP ها ، که با ایجاد سویه های نوترکیب پایدار قادر به رشد طولانی مدت در بیوراکتور هستند صورت می گیرد . هم اکنون برای تعداد زیادی از گونه ها، وکتور های الحاقی موثری در دسترس است که شامل مخمر هایی مثل پیکیاپاستوریس ، کلوودومایسس لاکتیس و قارچ های رشته ای آسپرژیلوس نیدولانس و نوروسپراکراسا می باشد.
وکتورهای کلونینگ برای گیاهان عالی
توسعه وکتورهای کلونینگ برای گیاهان عالی در دهه 1980 صورت گرفت به طوری که استفاده از آن ها منجر به تولید محصولات زراعی تغییر یافته ژنتیکی (GM) شد.
آگروباکتریوم تومه فاشینس – به عنوان کوچکترین مهندس ژنتیک طبیعت
اگرچه پلاسمیدهای طبیعی در گیاهان عالی شناسایی نشده اند، یک پلاسمید باکتریایی به نام Ti ، حاصل از آگروباکتریوم تومه فاشینس، دارای اهمیت زیادی است.
آگروباکتریوم تومه فاشینس یک میکروارگانیسم ساکن خاک است که در بسیاری از گیاهان دولپه ای ایجاد بیماری گال تاجی می کند. بیماری گال تاجی زمانی ایجاد می شود که تهاجم باکتری آگروباکتریوم تومه فاشینس از طریق زخم روی ساقه گیاه صورت بگیرد، که پس از آن باکتری باعث تکثیر سرطانی ساقه در محل تاج می شود.
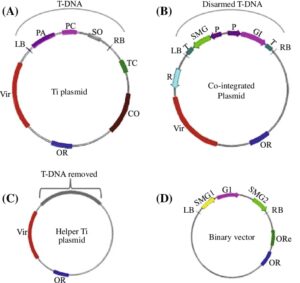
توانایی باکتری آگروباکتریوم تومه فاشینس مربوط به حضور پلاسمید Ti ( القا کننده تومور) در سلول هایش می باشد. این پلاسمید اندازه ای بزرگ تر از kb 200 دارد که حاوی تعداد زیادی از ژن های درگیر در فرایند آلودگی است. ویژگی قابل توجه این پلاسمید این است که بخشی از مولکول DNA خود را پس از آلود کردن گیاه به درون DNA کروموزوم گیاه وارد می کند.
این قطعه T-DNA نامیده می شود که بسته به سویه باکتری اندازه ای بین 15 و 30 کیلوباز دارد. این قطعه به شکل پایدار و به عنوان بخش کاملی از کروموزوم در سلول گیاه حفظ و به سلول های دختر منتقل می شود; اما برجسته ترین ویژگی پلاسمید Ti حضور 8 یا تعداد بیشتری ژن در T-DNA می باشد. که این ژن ها با بیان در سلول گیاهی باعث ویژگی های سرطانی در سلول های ترانسفورم شده می شوند. این ژن همچنین ترکیبات غیر معمولی که اوپین نامیده می شوند را جهت تغذیه باکتری سنتز می کنند.
استفاده از پلاسمید Ti جهت ورود ژن های جدید به سلول گیاهی
با کشف این پلاسمید سریعا مشخص شد که می توان از آن جهت انتقال ژن های جدید به داخل سلول های گیاهی استفاده کرد. برای این کار نیاز است که ژن های جدید درون T-DNA قرار گیرند و باکتری نیز کار دشوار ورود ژن ها به DNA کروموزوم گیاهی را انجام دهد.
دو روش ابداع شده برای ورود DNA جدید به داخل پلاسمید وجود دارد:
روش وکتور دوگانه: بر اساس مشاهداتی است که نیاز به اتصال فیزیکی T-DNA به بقیه پلاسمید Ti نیست. در این سیستم دو پلاسمیدی، T-DNA روی یک مولکول نسبتا کوچک و بقیه پلاسمید به شکل طبیعی وجود دارد. در چنین روشی کارایی انتقال به گیاه به اندازه سیستم طبیعی است. در حقیقت برخی از سویه های آگروباکتریوم تومه فاشینس و آگروباکتریوم های وابسته، دارای سیستم های پلاسمیدی دوگانه هستند. پلاسمید T-DNA برای داشتن یک جایگاه محدودالاثر منحصربه فرد و دست ورزی با استفاده از تکنیک های استاندارد به اندازه کافی کوچک است.
روش هم الحاقی: با استفاده از یک پلاسمید کاملا جدید مبتنی بر وکتور E.coli که حامل بخش کوچکی از T-DNA می باشد انجام می گیرد. همولوژی بین مولکول جدید و پلاسمید Ti این امکان را فراهم می آورد که چنانچه هر دو آن ها در یک آگروباکتریوم تومه فاشینس حضور داشته باشند. نوترکیبی باعث ورود پلاسمید E.coli به محل T-DNA پلاسمید Ti شود; بنابراین، برای این کار باید ژن کلون شده درون جایگاه محدودالاثر منحصربه فردی بر روی پلاسمید کوچک E.coli الحاق شود و سپس وارد سلول های آگروباکتریوم تومه فاشینس دارای Ti گردد. فرآیند نوترکیبی باعث قرار گیری ژن جدید در درون T-DNA می شود. با آلوده کردن گیاه، ژن جدید همراه با بقیه T-DNA به درون کروموزوم های گیاهی وارد می شود.
تولید گیاهان ترانسفورم شده با پلاسمید Ti
اگر باکتری آگروباکتریوم تومه فاشینس که حاوی پلاسمید Ti دستکاری شده است، به روش طبیعی وارد گیاه شود (مثل آلوده کردن زخم روی ساقه توسط باکتری)، فقط سلول های گال تاجی حاصل دارای ژن های کلون شده خواهند بود. برای حل این مشکل چندین راه حل وجود دارد، ساده ترین راه این است که به جای آلوده کردن گیاه بالغ، کشت سلول های گیاهی یا پروتوپلاست ها را در محیط مایع آلوده کرد.
با سلول های گیاهی و پروتوپلاست هایی که دیواره سلولی آن ها دوباره شکل گرفته است، می توان مانند میکروارگانیسم ها رفتار کرد. برای مثال می توان آن ها را در محیط کشت انتخابی به منظور جدا کردن سلول های ترانسفورم شده کشت داد. گیاه بالغی که از سلول های ترانسفورم شده باززایی می شود، در هر سلول خود حاوی ژن کلون شده خواهد بود که قادر است این ژن های کلون شده را به نسل بعدی منتقل کند.
باززایی گیاه ترانسفورم شده زمانی اتفاق می افتد که وکتور Ti خلع سلاح شده باشد که با این کار سلول های ترانسفورم شده خصوصیات سرطانی را نشان نمی دهند. خلع سلاح همه ی ژن های سرطانی که در T-DNA قرار گرفته اند امکان پذیر می باشد چون این ژن ها در روند آلوده سازی نقشی ندارند و آلوده سازی عمدتا توسط منطقه بیماری زایی پلاسمیدTi کنترل می شود.
پلاسمید Ri
چندسالی هست که وکتورهای کلونینگ گیاهی مبتنی بر پلاسمید Ri آگروباکتریوم ریزوژنز نیز مورد توجه قرار گرفته اند. پلاسمید های Ri و Ti بسیار شبیه به هم هستند با این تفاوت مهم که انتقال T-DNA پلاسمید Ri به جای ایجاد بیماری گال تاجی باعث بیماری ریشه مویی در گیاه می شودکه ریشه در اثر تکثیر شدید پر شاخه می شود.
کلونینگ ژن ها در گیاهان با انتقال مستقیم ژن
اگرچه پلاسمید Ti همیشه به عنوان امیدوارکننده ترین سیستم برای کلونینگ در گیاهان مطرح بوده است اما محدودیت های طیف میزبان طبیعی آگروباکتریوم تومه فاشینس سبب ترغیب جستجوی روش های جایگزین برای انتقال DNA جدید به داخل سلول های گیاه شده است که یکی از این روش ها انتقال مستقیم ژن می باشد.
انتقال مستقیم ژن به داخل هسته
در سال 1984 که برای اولین بار انتقال مستقیم ژن انجام شد، مشاهده شد که اگرچه پلاسمید مارپیچ مضاعف باکتریایی در سلول گیاهی قادر به همانندسازی از روی خودش نیست ولی می تواند با استفاده از نوترکیبی به یکی از کروموزوم های گیاهی وارد شود. با وجود اینکه فرآیند نوترکیبی به صورت جزئی شناخته شده است ولی به احتمال زیاد متمایز و متفاوت از فرایندهای دخیل در ورود T-DNA است.