آشنایی با انواع مختلف روش های رنگ آمیزی باکتری ها
رنگ آمیزی باکتری ها با هدف بررسی و مشاهده آن ها با استفاده از میکروسکوپ نوری می باشد که به روشهای مختلف و با اهداف متفاوت از جمله تشخیص، شناسایی و افتراق سویه های باکتریایی انجام میگیرد. همچنین تفکیک برخی از باکتریها، با رنگآمیزی های اختصاصی و مشاهده اجزای باکتری همانند اسپور، کپسول ، فلاژل و… انجام میگیرد.
در این مقاله آموزشی جامع قصد داریم 4 مورد از مهمترین روش های رنگ آمیزی باکتری ها را بررسی نماییم. بنابراین پس از خواندن این مقاله، باید بدانیم کاربرد روش های رنگ آمیزی باکتری ها در آزمایشگاه میکروب شناسی چه کمکی به ما می کند؟
1- رنگ آمیزی گرم
رنگ آمیزی گرم یکی از روش های مهم رنگ آمیزی باکتری ها و از تکنیک های پایه و پر کاربرد در آزمایشگاه میکروبی است، که به طور روتین جهت مطالعه نمونه های مستقیم بالینی یا اسمیر کشت به کار می رود. در واقع رنگ آمیزی گرم اولین گام در تشخیص و افتراق باکتری هاست که بر اساس آن استراتژی تشخیصی مناسب اتخاذ می شود. با این روش می توانیم بسیاری از باکتری ها، قارچ ها و تک یاخته ها را رنگ آمیزی کرد ولی برخی از ارگانیسم ها از جمله ترپونیا، میکوپلاسما، کلامیدیا و ریکتزیا به دلیل اندازه کوچک و یا نقص در دیواره سلولی با این روش قابل شناسایی نیستند.
این روش رنگ آمیزی باکتری ها در سال 1884 توسط باکتریولوژیست دانمارکی به نام هانس کریستین گرم ابداع شد. این روش بر اساس توانایی یا عدم توانایی میکروارگانیسم ها در نگه داشتن رنگ کریستال ویوله پس از رنگ بری با الکل-استن طراحی شده است.
در باکتری های گرم منفی ضخامت لایه پپتید و گلیکان بسیار کمتر از باکتری های گرم مثبت است ولی در عوض یک لایه ضخیم لیپو ساکاریدی(LPS) بر روی آن قرار گرفته است، در حالی که باکتری های گرم مثبت فاقد آن می باشند. اکثر باکتری ها گرم منفی هستند در حالی که تعدادی از باکتری ها و همچنین مخمر ها و کپک ها گرم مثبت هستند.
ویدیو آموزشی رنگ آمیزی باکتری ها به روش گرم با زیرنویس اختصاصی داروینو
رنگ آمیزی گرم همانند سایر روش های رنگ آمیزی باکتری ها موجب تضاد و کنتراست بین باکتری و محیط اطراف آنها می شود و فراتر از اون با این تکنیک، باکتری ها با توجه به ساختمان دیواره سلولی به دو گروه بزرگ گرم مثبت و گرم منفی تقسیم می شوند.
در رنگ آمیزی گرم ابتدا رنگ کریستال ویوله به لایه پپتید و گلیکان نفوذ می کند، سپس محلول ید (لوگل) به عنوان تثبیت کننده رنگ اولیه عمل کرده و یک کمپلکس نامحلول با کریستال ویوله ایجاد می کند به طوری که در مرحله رنگ بری، باکتری های گرم مثبت که لایه پپتید و گلیکان ضخیمی دارند نسبت به از دست دادن رنگ مقاومت می کنند، در صورتی که در باکتری های گرم منفی بدلیل وجود لیپید در دیواره سلولی و حل شدن آن بوسیله مواد رنگ بر، کریستال ویوله را براحتی از دست می دهند.
در مرحله آخر رنگ آمیزی باکتری ها به روش گرم، فوشین یا سافرانین بعنوان رنگ مکمل یا متضاد افزوده می شود تا باکتری های بی رنگ (گرم منفی) را به رنگ قرمز رنگ آمیزی کند. در تصویر زیر خلاصه مراحل انجام رنگ آمیزی گرم را مشاهده می کنید.
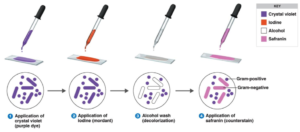
رنگ آمیزی باکتری ها – پروتکل/روش کار رنگ آمیزی گرم
برخی از خصوصیات باکتری های گرم مثبت و گرم منفی
- باکتری های گرم مثبت نسبت به پنی سیلین و مواد ضد باکتریایی حساس تر از باکتری های گرم منفی می باشند
- گرم مثبت بودن خاصیتی متغیر است ولی خاصیت گرم منفی تحت هیچ شرایطی از بین نمی رود، بنابراین در لام گرم مثبت ممکن است اجرام گرم منفی هم مشاهده شود ولی در لام گرم منفی هرگز باکتری گرم مثبت دیده نمی شود.
- باکتری های گرم منفی نسبت به باکتری های گرم مثبت سخت رشد تر هستند و نیاز های غذایی پیچیده تری دارند.
- باکتری های گرم منفی نسبت به اسید و قلیا حساس تر هستند.
- باکتری های گرم مثبت تحت تاثیر موادی همچون لیزوزوم و پنی سیلین دیواره سلولی خود را از دست داده و به پروتوپلاست تبدیل می شوند. پروتوپلاست ها سلول های بسیار شکننده ای بوده و تنها در محیط های ایزوتونیک( هم فشار) قادر به ادامه حیات می باشند. پروتوپلاسیت قابلیت سنتز دیواره سلولی را به طور کامل از دست می دهد.
- باکتری های گرم منفی با از دست دادن دیواره سلولی خود به اسفروپلاست تبدیل می شوند. اسفروپلاست قطعاتی از دیواره سلولی را در خود حفظ کرده و مجددا قادر به سنتز دیواره سلولی می باشد.
- اگر سلول های فاقد دیواره قابلیت رشد و تکثیر را حفظ کنند تحت عنوان اشکال L باکتری ها خوانده می شوند، این فرم از باکتری ها نقش بسزایی در عود مجدد بیماری های عفونی دارند.
2- رنگ آمیزی اسید فست(زیل نلسون)
در ابتدا بهتر است مقدمه ای مختصر در خصوص مایکوباکتریوم را مرور کنیم سپس رنگ آمیزی باکتری ها به روش اسید فست برای افتراق سویه های مختلف مایکوباکتریوم را بررسی نماییم.
مایکوباکتریوم ها به شدت هوازی هستند و رشد آهسته ای دارند. زمان دو برابر شدن باکتری(G.T) بطور متوسط 12 ساعت و در مورد باسیل سل 20 تا 22 ساعت می باشد. سریع ترین رشد مایکوباکتریوم ها در مدت 2 تا 3 روز است و مایکوباکتریوم های بیماریزا در طی 2 تا 6 هفته رشد می کنند. در محیط حاوی 5 تا 10 درصد دی اکسید کربن رشد بهتری انتظار می رود.
محیط های مناسب کشت برای مایکوباکتریوم ها:
- Egg Based Media: این محیط حاوی تخم مرغ، پودر سیب زمینی، گلیسرول، املاح و رنگ مالاشیت گرین است. مالاشیت گرین از رشد باکتری های گرم مثبت جلوگیری میکند.
- Serum or Agar Based Media: محیط های سرم آلبومین مانند محیط مید لبروگ آگار شامل نمک های مختلف، ویتامین ها، کوفاکتور ها و مالاشیت گرین می باشد که با اسید اولئیک و آلبومین گاوی غنی شده است. این محیط شفاف بوده و می توان با بزرگنماییی کم میکروسکوپ کلونی های اولیه را در محیط کشت شناسایی کرد.
- Liquid Media: در محیط های مایع گونه های مایکوباکتریوم می توانند سریعتر رشد کنند. محیط مید لبروگ براث جهت کشت مجدد سویه ای ذخیره استفاده می شود.
تست های تشخیصی مایکوباکتریوم ها:
برای تشخیص مایکوباکتریوم ها از بین روش های رنگ آمیزی باکتری ها، رنگ آمیزی اسید فاست انجام می شود، سپس نمونه را بر روی محیط های جامد، کشت می دهند و خصوصیات فنوتیپی مثل مورفولوژی، کلنی، سرعت رشد، دمای بهینه رشد، واکنش های بیوشیمیایی و پیگمنتاسیون نسبت به نور مورد بررسی قرار می دهند.
خصوصیات کلنی: مایکوباکتریوم ها به دلیل وجود فاکتور طنابی که باعث ایجاد رشته های خمیده باسیل می شود، کلنی خشک وخشن به رنگ سفید شیری تا کرم رنگ ایجاد می کنند
سرعت رشد: بسته به گونه مایکوباکتریوم از 3 تا 60 روز متغیر است.
واکنش در برابر نور:
- فتوکروموژن: گونه هایی هستند که در مجاورت نور رنگدانه های کاروتن تولید می کنند
- اسکوتوکروموژن: گونه هایی هستند که هم در تاریکی و هم در روشنایی رنگدانه تولید می کنند
- غیر کروموژن: گونه هایی هستند که در هیچ شرایطی قادر به تولید رنگدانه نیستند
تست های بیوشیمیایی: این تست ها به علت سرعت آهسته رشد ممکن است چندین هفته به طول بیانجامد همانند تست نیاسین، تست احیا نیترات، تست احیا تلوریت و …
ویدیو آموزشی رنگ آمیزی باکتری ها به روش اسید فست با زیرنویس اختصاصی داروینو
تکنیک رنگ آمیزی اسید فاست یک دیگر از روش های رنگ آمیزی باکتری هاست که برای اولین بار توسط Dr.Franz Ziehl و Dr.Friedrich Neelsen ابداع شد. واژه اسید فاست به معنی مقاوت در مقابل رنگ بری با یک رنگ بر قوی اسیدی است. این خاصیت در باکتری های جنس مایکوباکتریوم و نوکاردیا و تک یاخته کریپتوسپوریدیوم وجود دارد.
این روش از رنگ آمیزی باکتری ها، حضور مایکوباکتریوم در نمونه های بالینی را بررسی می کند و می توان از طریق آن سویه های مختلف مایکوباکتریوم از جمله مایکوباکتریوم توبرکلروزیس(عامل بیماری سل)، مایکوباکتریوم اولسرانس(عامل اولسر بورولی) و مایکوباکتریوم لپره(عامل جذام) را شناسایی کرد.
مایکوباکتریوم ها باسیل های بدون حرکت و بدون اسپور می باشند که در دیواره سلولی خود علاوه بر پپتید و گلیکان مقادیر زیادی گلیکولیپید بویژه اسید میکولیک دارند، بطوریکه 60 درصد دیواره سلولی باکتری را اسید میکولیک تشکیل میدهد.
دیواره سلولی این باکتری ها شبیه موم بوده و نسبتا غیر قابل نفوذ است. اسید میکولیک و سایر گلیکولیپید ها نفوذ مواد شیمیایی مورد نیاز برای رشد باکتری را آهسته می کند، همچنین باکتری را در مقابل عوامل شیمیایی باکتری کش و ترکیبات لیزوزومی محافظت می کنند. حتی این باکتری ها را در مقابل خشکی مقاوم می سازد. با این وجود باسیل سل توسط پاستوریزاسیون و سترون سازی عادی توسط حرارت به آسانی از بین می رود.مایکوباتریوم ها به شدت هوازی هستند و رشد بسیار آهسته ای دارند. زمان دو برابر شدن باکتری 18 ساعت است.
برای انجام این تست بعد از جمع کردن نمونه مورد نظرتون، برای تغلیظ نمونه از سانتریفیوژ با سرعت 3000g به مدت 15 دقیقه استفاده کرده. با این کار مایکوباکتریوم ها در انتهای لوله جمع شده و پس از خالی کردن محلول رویی، از رسوب حاصل برای کشت و رنگ آمیزی استفاده شده.
باکتری های اسید فاست به دلیل داشتن دیواره مومی، تقریبا نفوذ ناپذیر بوده و به سادگی با رنگ های روتین رنگ نمی شوند بنابراین سایر روش های رنگ آمیزی از جمله گرم کاربردی ندارند.

برای یادگیری انواع روش های رنگ آمیزی باکتری ها و سایر تکنیک های کارآموزی میکروبیولوژی
از طریق لینک دوره های آموزشی تخصصی آزمایشگاه می توانید اقدام نمایید.
-
رنگ کربول فوشین محلول در چربی است، همچنین دارای فنول می باشد که نفوذ رنگ به داخل دیواره سلولی را تسهیل می کند. این فرایند طی سه مرحله انجام می شود:
مرحله اول: رنگ آمیزی اولیه است که در رنگ کربول فوشین را جهت نفوذ بهتر به دیواره سلولی مومی مایکوباکتریوم حرارت می دهیم که این موضوع سبب اتصال رنگ به اسید مایکولیک دیواره سلولی می شود
مرحله دوم: رنگ زدایی است که در این مرحله با استفاده از محلول ضد رنگ سلول های پس زمینه بافت و هر ارگانیسم دیگر موجود در اسمیر به جز مایکوباکتریوم رنگ زدایی می شوند.
مرحله سوم: رنگ آمیزی با متضاد رنگ اولیه است. با اضافه کردن متیلن بلو، تمام مواد بک گراند آبی رنگ می شود و به واسطه این رنگ متضاد باسیل های اسید فست به رنگ قرمز دیده می شوند.

رنگ آمیزی باکتری ها – پروتکل/دستورالعمل انجام رنگ آمیزی اسید فست
اسمیر رنگ شده با رنگ بر های بسیار قوی (اسید کلریدریک 3 درصد و اتانول 95 درصد) رنگ زدایی نمی شود و رنگ اولیه را حفظ می کند، در این پروسه جهت رنگ آمیزی باکتری های غیر اسید فاست که رنگ اولیه را از دست دادند، از رنگ متضاد متیلن بلو استفاده می شود. در این تکنیک باکتری های اسید فاست به رنگ قرمز و مواد زمینه و سایر باکتری ها به رنگ آبی مشاهده می شوند.
روش دیگر برای مشاهده مایکوباکتریوم ها استفاده از رنگ اورامین و رودامین است، با این روش باکتری ها رنگ فلوئورسنت را جذب کرده و با اسید آن را از دست نمی دهند. در مشاهده باکتری ها، به صورت نقاط نورانی در یک زمینه سیاه دیده می شوند در این روش مدت زمان کمتری برای مطالعه اسلاید صرف شده است.

3- رنگ آمیزی اندوسپور
در ابتدا نیاز است مقداری به بررسی ساختار اسپور بپردازیم
برخی از باکتری ها قادرند با تشکیل ساختار های مقاوم بنام اندوسپور شرایط سخت محیطی را تحمل کنند و در شرایط مناسب مجددا به فرم رویشی تبدیل بشوند. تولید اسپور در واقع یک نوع تمایز سلولی است زیرا که در این فرایند آنزیم ها و ساختمان های جدید جایگزین آنزیم ها و ساختمان های قبلی می شوند، بطوریکه آنتی ژن های مخصوص در مرحله اسپورولاسیون تولید می شود در حالی که در مرحله فعال باکتری وجود ندارد. شرایط تغذیه ای نامناسب از جمله؛ تخلیه منابع کربن و نیتروژن مهمترین عوامل تولید اسپور می باشند، همچنین کمبود مواد انرژی زا، سولفات، فسفات و آهن تشکیل اسپور را تحریک می کنند.
اسپور یا اندوسپور در واقع مرحله استراحت و شکل مقاوم باکتری می باشد. همه باکتری ها قادر به تولید اسپور نیستند. باسیلوس ها و کلستریدیوم ها دو جنس مهم باکتریایی تولید کننده اسپور می باشند. سایر گونه های اسپور زا اسپوروسارسینا و کوکسیلابورنتی هستند.
به طور کلی موقعیت قرار گرفتن اسپور در سلول مادر به سه حالت؛ مرکزی(Central) ، انتهایی(Terminal) و نزدیک انتهایی(Subterminal) می باشد و شکل اسپورهم به صورت کروی (Spherical) و بیضی(Oval) مشاهده می شود. اندازه اسپور کلستریدیم ها بزرگتر از سلول والد بوده و موجب تورم و تغییر شکل سلول مادر می شود ولی اندازه اسپور در جنس باسیلوس ها کوچکتر از سلول والد می باشد.
ساختمان اسپور
Core: پروتوپلاست اسپور است که حاوی یک هسته کامل ( کروموزوم) و تمام اجزاء سیستم تولید پروتئین و یک سیستم تولید انرژی از طریق گلیکولیز می باشد. انرژی مورد نیاز اسپور بیشتر بصورت 3-فسفوگلیسرات ذخیره می شود.
Inner membrane: داخلی ترین لایه اطراف اسپور را تشکیل می دهد.
Germ cell wall: دیواره اسپور، غشاء داخلی اسپور را احاطه می کند. این دیواره از پپتید وگلیکان معمولی تشکیل شده و دیواره سلولی باکتری فعال و زایای بعدی را تشکیل می دهد.
Cortex: کورتکس ضخیم ترین لایه پوشش اسپور است. این لایه از نوعی پپتید وگلیکان غیر معمول ساخته شده است که تعداد پل های عرضی آن از پپتید وگلیکان دیواره سلولی بسیار کمتر است. این لایه به شدت نسبت به لیزوزیم حساس بوده و اتولیز آن در زایا شدن نقش دارد.
Outer membrane: این لایه از یک پروتئین شبه کراتینی با پیوند های دی سولفیدی زیاد ساخته شده است. مقاومت نسبی اسپور در برابر عوامل شیمیایی مربوط به نفوذ ناپذیری این لایه می باشد.
Exosporium: اگزواسپور خارجی ترین لایه بوده و از جنس لیپوپروتئین است.
ویدیو آموزشی رنگ آمیزی اسپور باکتری ها با زیرنویس اختصاصی داروینو
روش رنگ آمیزی اندوسپور
اندوسپور به دلیل نفوذ ناپذیر بودن به آسانی رنگ نمی گیرد و در صورت رنگ پذیری به آسانی رنگ خود را از دست نمی دهد. این خاصیت اساس و پایه رنگ آمیزی اسپور را تشکیل می دهد. اسپور به وسیله رنگ مالاشیت گرین و با کمک حرارت رنگ آمیزی می شود، سپس سافرانین به عنوان رنگ مکمل در این تکنیک مورد استفاده قرار می گیرد. در این روش باکتری ها قرمز رنگ و اندوسپور ها به رنگ سبز در داخل پیکر باکتری والد مشاهده می شوند.
اگر باکتری اسپور دار به روش گرم رنگ آمیزی شود اندوسپور ها به صورت مناطق شفافی قابل مشاهده خواهند بود. همچنین اندوسپور را می توان به علت شفافیت با میکروسکوپ فازکنتراست مشاهده کرد.
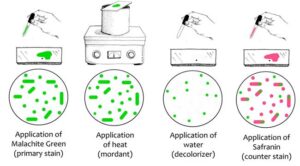
رنگ آمیزی باکتری ها – پروتکل/دستورالعمل رنگ آمیزی اندوسپور
4- رنگ آمیزی کپسول
کاربردهای رنگ آمیزی کپسول و رنگ آمیزی باکتری گرم منفی:
رنگ آمیزی منفی جهت بررسی میکروسکوپی باکتری های کپسول دار کاربرد دارد. بسیاری از باکتری های مهم پزشکی از جمله استرپتوکوک پنومونیه، باسیلوس آنتراسیس و تعدادی از قارچ ها مثل کریپتوکوکوس نئوفورمنس یک پوشش خارجی بنام کپسول دارند. مشاهده کپسول در میکروارگانیسم بعنوان معیار تشخیصی و فاکتور بیماریزا دارای اهمیت زیادی است.
رنگ آمیزی کپسول روش نسبتا مشکلی است، زیرا مواد کپسولی محلول در آب بوده و ممکن است بوسیله شستشو از بین برود. همچنین حرارت نیز باعث تخریب ساختار کپسول می شود. کپسول به حدی متراکم و محدود نیست که بتوان آن را در رنگ آمیزی عادی مشاهده کرد، لذا از رنگ آمیزی منفی برای مشاهده آن مشاهده می شود. در رنگ آمیزی منفی، زمینه با استفاده از رنگ های اسیدی رنگ می گیرد ولی کپسول باکتری بدون رنگ می ماند. در این روش کپسول بصورت هاله ای شفاف در اطراف باکتری و در یک زمینه تاریک مشاهده می شود.
رنگ آمیزی کپسول به روش های مختلفی انجام می شود:
- روش آنتونی(Anthony)
- روش گراهام-اوانس (Graham and Evans)
- رنگ آمیزی منفی (نیگروزین)
برای مطالعه پروتکل مربوط به انواع روشهای رنگ آمیزی کسپول مقاله جامع دستورالعمل رنگ آمیزی کپسول و رنگ آمیزی باکتری گرم منفی بخوانید.

برای دریافت خدمات آزمایشگاه میکروبیولوژی و انجام انواع تست های رنگ آمیزی باکتری ها
از طریق لینک خدمات آزمایشگاهی می توانید اقدام نمایید
-
نکاتی که در حین تمامی انواع رنگ آمیزی کپسول باکتری ها باید رعایت شود:
- در تمامی مراحل تهیه اسمیر و رنگ آمیزی کپسول به جای آب از محلول سولفات مس استفاده شود؛ زیرا کپسول باکتری از جنس پلی ساکارید بوده و در آب حل می شود.
- از هم زدن زیاد توسط لوپ خودداری کنیم؛ زیرا کپسول باکتری نسبتا شل بوده و ممکن است از باکتری جدا شود و متلاشی گردد.
- در رنگ آمیزی کپسول فیکس کردن بوسیله حرارت انجام نمی گیرد؛ برای اینکه حرارت باعث چروکیدن و بدشکل شدن سلول باکتری شده، همچنین موجب از بین رفتن کپسول می شود.
- استفاده از مقدار بسیار کمی جوهر هندی باعث شده تا کپسول بهتر مشاهده شود
- به یاد داشته باشید همواره باید اسمیر عاری از هرگونه روغن، چربی و اثر انگشت باشد در غیر این صورت بهتر است اسلاید دیگری تهیه شود.
بیشتر بخوانید:










































