آزمایش OF – اکسیداسیون یا تخمیر گلوکز
✍ پروتکل/دستورالعمل آزمایش OF – تشخیص هوازی یا بی هوازی بودن باکتری
غالبا آب و خاک بوده و بر روی مخاط بدن انسان و حیوانات نیز زندگی می کنند. این باکتری ها همچنین از محیط های مرطوب مانند وسایل کمک تنفسی، حمام، شیر آب و حتی محلول های ضدعفونی کننده جدا شده اند. در حضور مواد شیمیایی ضدعفونی کننده قادر به رشد بوده و به علت مقاومت آنتی بیوتیکی از اهمیت خاصی برخوردارند.
مهمترین باکتری های این گروه عبارتند از؛ پسودوموناس، اسینتوباکتر، آلکالیژنز، کروباکتر، موراکسلا از مهمترین عوامل شایع در عفونت های بیمارستانی پسودوموناس ائروژینوزا می باشد.
| نام باکتری | عمق TSI | O/F glucose | اکسیداز | همولیز کامل | پیگمانتاسیون | |
| بسته | باز | |||||
| پسودوموناس | بدون تغییر | – | + | + | + | + |
| اسنیتوباکتر | بدون تغییر | – | +/- | – | – | – |
| الکالیژنز | بدون تغییر | – | – | + | – | – |
| انتروباکتریاسه | زرد | + | + | – | +/- | – |
باسیل های گرم منفی غیرتخمیری فاقد اسپور، هوازی وغالبا متحرک می باشد. در شرایط بی هوازی فقط نمونه هایی رشد می کنند که قادر به استفاده از نیترات یا آرژنین به عنوان گیرنده نهایی الکترون باشند.
در بررسی های آزمایشگاهی، ابتدا باید آنها را از انتروباکتریاسه تشخیص داد. انتروباکتریاسه ها همگی اکسیداز منفی می باشند ولی در مقابل باسیل های گرم منفی غیر تخمیر کننده اکسیداز مثبت یا منفی می باشند. آزمایش اکسیداز، توانایی رشد در محیط مک کانکی آگار، توانایی استفاده از کربوهیدرات ها و نوع مسیر متابولیکی که توسط میکروارگانیسم مورد استفاده قرار می گیرد. برای تشخیص جنس باکتری در ابتدا از چند آزمایش استفاده می شود که عبارتند از:
-
آزمایش OF
یکی از مهمترین خصوصیات افتراقی باکتری های گرم منفی غیر تخمیری از انتروباکتریاسه، توانایی ارگانیسم در استفاده از کروبوهیدرات ها می باشد. در این آزمایش از محیطی به نام Oxidative Fermentative Media که دارای مقادیر بسیار کمی پیتون است، استفاده می شود. هرچند محیط TSI و یا KIA تخمیر و عدم تخمیر قند را نشان می دهد، ولی به علت بالا بودن مقدار پیتون در محیط، مقادیر کم اسید خنثی می شود. بنابراین پاسخ درستی ارائه نمی گردد. ولی محیط OF دارای پیتون کم و مقدار بیشتری کربوهیدرات است. کاهش میزان پروتئین، تولید آمین های قلیایی را که مقادیر اندک اسید ناشی از اکسیداسیون قند را خنثی می کنند، کاهش داده و در نتیجه تولید مقدار کم اسید نیز مشخص می شود. همچنین با افزایش نسبی میزان قند محیط کشت OF مقدار اسید حاصل از اکسیداسین افزایش می یابد. در محیط کشت OF قدرت تحرک باکتری نیز مشخص می گردد.
برای کشت بر روی این دو محیط از دو لوله استفاده می شود. ارگانیسم جدا شده را در هر دو محیط تلقیح کرده و سپس یکی از محیط ها را با پارافین استریل پوشانده که شرایط بی هوازی ایجاد شود.
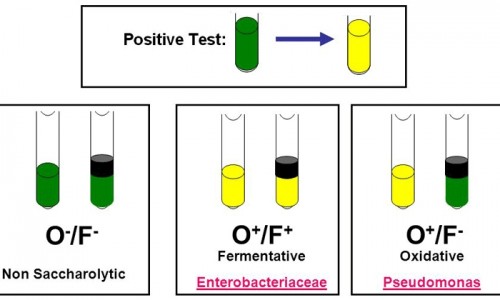
بعد از انکوباسیون در لوله هایی که رنگ زرد ایجاد شده، اسید تولید و گلوکز مصرف شده است.در لوله واجد پارافین (شرایط بی هوازی) عمل تخمیر و در لوله ی فاقد پارافین (شرایط هوازی) عمل اکسیداسیون صورت می گیرد.
این محیط دارای قند گلوکز و معرف برموتیمول بلو می باشد. اگر گلوکز محیط مصرف شود، اسید تولید می شود و برموتیمول بلو از حالت سبز به زرد تغییر رنگ می دهد. اگر هر دو لوله (با یا بدون روغن) زرد شود، میکروارگانیسم بی هوازی اختیاری می باشد، یعنی توانایی استفاده از گلوکز را در حضور یا عدم حضور اکسیژن دارد. در صورتی که فقط در لوله بدون روغن رنگ زرد ایجاد شود، باکتری هوازی است و توانایی استفاده از گلوکز را تنها در حضور اکسیژن دارا می باشند. عدم تغییر رنگ در لوله نشانه این است که میکروارگانیسم قادر به مصرف گلوکز نمی باشد.
پروتکل/روش انجام آزمایش
- تهیه اسمیر از کشت و رنگ آمیزی گرم
مقدار کمی از کلونی را با اپلیکاتور، آنس یا لوپ برداشته و با یک قطره سالین یا آب مقطر استریل بر روی لام مخلوط کنید تا سوسپانسیون یکنواختی حاصل گردد. اسمیر را در مجاورت هوا خشک کنید. سپس به وسیله حرارت آن را فیکس کرده و رنگ آمیزی گرم را انجام دهید.
- کشت بر روی آگار خونی جهت بررسی همولیز و رنگدانه
باکتری مورد نظر را در شرایط استریل به روش خطی بر روی محیط کشت آگار خونی تلقیح نموده و به مدت ۲۴ ساعت در دمای ۳۵ درجه سانتیگراد نگهداری کنید. پس از طی دوره انکوباسیون کلونی باکتری ها را از نظر نوع همولیز و رنگ کلونی مورد بررسی قرار دهید.
- کشت پسودوموناس آئروژینوزا در ژلوز ساده در لوله برای مشاهده پیگمان
از پسودوموناس برداشت کرده و بر روی پلیت نوترینت آگار بصورت خطی کشت دهید. این باکتری پیگمن های مختلفی ترشح می کند از جمله پیوسیانین که آبی رنگ است و فلوئورسئین که زرد مایل به سبز می باشد. این پیگمان ها در آب محلول بوده و روی محیط ژلوز منتشر می شوند و پس از ۷۲ ساعت محیط را به رنگ آبی مایل به سبز در می آورند.
- کشت عمقی و سطحی در محیط TSI
در شرایط استریل و با استفاده از آنس نوک تیز(نیدل) عمق لوله را بصورت خط عمود و سطح شیبدار را بصورت زیگزاگ کشت دهید. به مدت ۱۸ تا ۲۴ ساعت در دمای ۳۵ درجه سانتیگراد نگهداری کنید. پس از سپری شدن زمان انکوباسیون لوله ها را از نظر واکنش های مختلف بیوشیمیایی مورد بررسی قرار دهید.
- آزمون اکسیداسیون-فرمانتاسیون
نمونه مورد آزمایش را به ۲ لوله محیط کشت OF تلقیح کنید و سطح یکی از لوله ها را با لایه ای به ضخامت یک سانتیمتر از یک روغن معدنی یا پارافین ذوب شده بپوشانید تا شرایط بی هوازی ایجاد گردد. لوله دیگر را در شرایط هوازی انکوبه کنید. هر دو لوله را بر حسب باکتری مورد آزمایش به مدت چند روز در دمای ۳۵ درجه سانتیگراد نگهداری کنید. پس از سپری شدن دوره انکوباسیون نمونه ها را از نظر تغییر رنگ و نوع واکنش محیط بررسی نمایید.
- تست اکسیداز
یک کاغذ صافی تمیز را در سطح یک پلیت استریل پلاستیکی قرار داده و آن را با چند قطره از معرف تازه مرطوب نمایید. مقدار کمی از کلونی جوان (کمتر از ۲۴ ساعت) را با استفاده از یک اپلیکاتور چوبی تمیز برداشته و بر روی کاغذ صافی مرطوب شده قرار دهید. از نظر تغییر رنگ کلونی ها به رنگ آبی و بنفش در مدت ۱۰ تا ۲۰ ثانیه بررسی کنید.
نکات مهم در حین انجام آزمایش
- به منظور دستیابی به نتایج صحیح TSI را طی ۱۸ تا ۲۴ ساعت پس از انکوباسیون مورد بررسی قرار دهید، زیرا در طی این فاصله زمانی هرگز سوبسترا قندی باکتری تمام نشده و باکتری برای تامین انرژی خود از پیتون ها استفاده نکرده است. توجه داشته باشید در تست اکسیداز تغییر رسوب سواب ۲۰ تا ۳۰ ثانیه بعد از زمان افزودن معرف ارزش تشخیصی ندارد.
- استفاده از میله فلزی (نیکل-کروم) در نتیجه آزمایش اکسیداز تداخل ایجاد کرده و نتیجه مثبت کاذب می دهد.
- سواب ها و اپلیکاتور های مصرف شده را بلافاصله در ظروف حاوی مواد ضدعفونی کننده قرار دهید.
- در آزمون OF زمان انکوباسین باکتری های کند رشد را می توان به مدت طولانی تری ادامه داد.
نوشته شده توسط کارگروه تولید محتوا در تاریخ ۹۹/۰۵/۲۶ ساعت ۳:۰۵ ق٫ظ | تعداد دیدگاهها: ۰ دیدگاه | دستهبندی: بلاگ | برچسبها: آزمایش_OF, آزمون_اکسیداسیون_فرمانتاسیون, آلکالیژنز, اسینتوباکتر, بررسی_خصوصیات_و_کشت_و_واکنش_های_باکتری_های_گرم_منفی_غیر_تخمیر_کننده, تست_اکسیداز, خصوصیات_کشت_و_واکنش_های_باکتری_های_گرم_منفی_غیر_تخمیر_کننده, راهنمای-آموزشی_خصوصیات_کشت_و_واکنش_های_باکتری_های_گرم_منفی_غیر_تخمیر_کننده, رفع_اشکالات_خصوصیات_کشت_و_واکنش_های_باکتری_های_گرم_منفی_غیر_تخمیر_کننده, روش_انجام_آزمایش_تهیه_اسمیر_از_کشت_و_رنگ_آمیزی_گرم, فایل_pdf_خصوصیات_کشت_و_واکنش_های_باکتری_های_گرم_منفی_غیر_تخمیر_کننده, موراکسلا, پسودوموناس, کروباکتر, کشت_بر_روی_آگار_خونی_جهت_بررسی_همولیز_و_رنگدانه, کشت_عمقی_و_سطحی_در_محیط_TSI, کشت_پسودوموناس_آئروژینوزا_در_ژلوز_ساده_در_لوله_برای_مشاهده_پیگمان